题目内容
水与人类的生活和生产密切相关.某实验小组发现实验室中得到的自来水呈黄色,有异味,且水样浑浊,有固体小颗粒.现对水样进行如下处理:
①向水样中加入明矾,搅拌溶解,静置沉淀后,进行
②向上述清液中加入活性炭,利用其
③欲检验水样是否显酸性,可选用
④小组同学利用一种新型的自来水消毒剂X,对水进行消毒.工业上制取X 的化学方程式为:Cl2+2NaClO2═2NaCl+2X,则X的化学式为
⑤依据上述反应,若有2molCl2 参与反应,则可产生NaCl
①向水样中加入明矾,搅拌溶解,静置沉淀后,进行
过滤
过滤
(填操作名称),可得到清液;②向上述清液中加入活性炭,利用其
吸附
吸附
作用除去水样中的颜色和异味,该过程属于物理
物理
变化(填“物理”或“化学”).③欲检验水样是否显酸性,可选用
石蕊试液
石蕊试液
或pH试纸
pH试纸
.④小组同学利用一种新型的自来水消毒剂X,对水进行消毒.工业上制取X 的化学方程式为:Cl2+2NaClO2═2NaCl+2X,则X的化学式为
ClO2
ClO2
,NaClO2中氯元素的化合价为+3
+3
.⑤依据上述反应,若有2molCl2 参与反应,则可产生NaCl
234
234
克.(写出列式计算的过程)分析:根据已有的知识进行分析,过滤时分离不溶性固体和液体的方法,活性炭具有吸附性,能吸附色素和异味,要检验溶液的酸碱性,可以使用酸碱指示剂或pH试纸;根据质量守恒定律,化学反应前后元素的种类和原子的个数不变,可以推得X的化学式,根据化合价规则可以求得化合物中某元素的化合价;根据反应的化学方程式可以求出参加反应的氯化钠的物质的量,再求出其质量.
解答:解:①要除去水中的不溶性固体,可以使用过滤的方法,故填:过滤;
②活性炭具有吸附性,能吸附色素和异味,此过程中没有生成新的物质,属于物理变化,故填:吸附,物理;
③检验水样是否呈酸性,可以根据酸的性质进行,酸性溶液能使石蕊试液变红,酸性溶液的pH小于7,故填:石蕊试液,pH试纸;
④依据反应的化学方程式,Cl2+2NaClO2═2NaCl+2X,反应前含有4个Cl原子,2个Na原子,4个O原子,反应后已有2个Na原子,2个Cl原子,故2X中含有2个Cl原子和4个O原子,故X中含有1个Cl原子和2个O原子,其化学式为ClO2,
设氯元素的化合价为x,则有(+1)+x+(-2)×2=0,解得x=+3,
故填:ClO2,+3;
⑤设生成氯化钠的物质的量为x
Cl2+2NaClO2═2NaCl+2ClO2
1 2
2mol x
=
x=4mol
氯化钠的质量为4mol×58.5g/mol=234g
故填:234.
②活性炭具有吸附性,能吸附色素和异味,此过程中没有生成新的物质,属于物理变化,故填:吸附,物理;
③检验水样是否呈酸性,可以根据酸的性质进行,酸性溶液能使石蕊试液变红,酸性溶液的pH小于7,故填:石蕊试液,pH试纸;
④依据反应的化学方程式,Cl2+2NaClO2═2NaCl+2X,反应前含有4个Cl原子,2个Na原子,4个O原子,反应后已有2个Na原子,2个Cl原子,故2X中含有2个Cl原子和4个O原子,故X中含有1个Cl原子和2个O原子,其化学式为ClO2,
设氯元素的化合价为x,则有(+1)+x+(-2)×2=0,解得x=+3,
故填:ClO2,+3;
⑤设生成氯化钠的物质的量为x
Cl2+2NaClO2═2NaCl+2ClO2
1 2
2mol x
| 1 |
| 2mol |
| 2 |
| x |
x=4mol
氯化钠的质量为4mol×58.5g/mol=234g
故填:234.
点评:本题考查了净水的知识以及质量守恒定律的应用,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
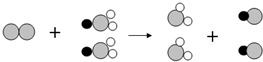
 表示氯原子,
表示氯原子, 表示钠原子,
表示钠原子, 表示氧原子)
表示氧原子)
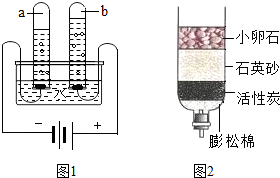 2012年3月22日是第二十届“世界水日”.水与人类的生活和生产密切相关.
2012年3月22日是第二十届“世界水日”.水与人类的生活和生产密切相关. 水与人类的生活和生产密切相关.请回答下列问题.
水与人类的生活和生产密切相关.请回答下列问题.