题目内容
【题目】课外小组同学进一步研究铁与氧气的反应。
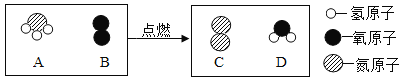
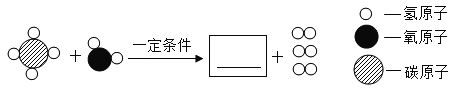
(提出问题)铁丝燃烧时为什么会有“火星四射”的现象?
(查阅资料)铁丝燃烧时“火星四射”现象与铁丝含碳量有关。
(进行实验)探究铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系。
实验 | 现象 | 解释与结论 |
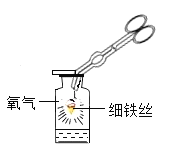
实验1:取直径0.20mm、含碳0.1%的铁丝,在氧气中燃烧 | 零星的火星四射 | ①写出铁丝燃烧的化学方程式_____ ②0.20mm的铁丝在氧气中燃烧,“火星四射”与其含碳量的关系为_____ |
实验2:取直径0.20mm、含碳0.32%的铁丝,在氧气中燃烧 | 较明显的火星四射 | |
实验3:取直径0.20mm、含碳0.52%的铁丝,在氧气中燃烧 | _____ |
(提出问题)纯铁在氧气中燃烧溅落的“黑色固体”是什么?
(查阅资料)
①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO易被氧化)
②铁的氧化物均能溶于酸溶液
(进行实验)测定黑色固体的成分。
实验 | 现象及数据 | 解释与结论 |
实验4:将冷却后的黑色固体碾碎,装入试管,加入_____溶液 | 固体溶解且有气泡产生 | 铁燃烧时溅落下来的黑色固体中含有_____。 |
实验5:取2.8g纯铁在氧气中燃烧,收集溅落的黑色固体,干燥并称其质量 | 黑色固体质量为3.44g | 黑色固体的组成及质量为_____。 |
【答案】3Fe+2O2 Fe3O4 在实验范围内当其他条件都相同时,含碳量越高火星四射越剧烈 大量火星四射 稀盐酸 铁 Fe:1.12g;Fe3O4:2.32
Fe3O4 在实验范围内当其他条件都相同时,含碳量越高火星四射越剧烈 大量火星四射 稀盐酸 铁 Fe:1.12g;Fe3O4:2.32
【解析】
实验1:
铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为:3Fe+2O2 Fe3O4;
Fe3O4;
实验2:
根据表格中的数据和实验现象,0.20mm的铁丝在氧气中燃烧,“火星四射”与其含碳量的关系为在实验范围内当其他条件都相同时,含碳量越高火星四射越剧烈;
实验3:
直径0.20mm、含碳0.52%的铁丝中含碳量大于0.20mm、含碳0.32%的铁丝。根据实验①②的结论可知,实验3中直径0.20mm、含碳0.52%的铁丝,在氧气中燃烧大量火星四射;
实验4:
铁与盐酸反应生成氯化亚铁和氢气,因此:
实验 | 现象及数据 | 解释与结论 |
实验4:将冷却后的黑色固体碾碎,装入试管,加入稀盐酸溶液 | 固体溶解且有气泡产生 | 铁燃烧时溅落下来的黑色固体中含有铁。 |
实验5:
设参加反应的铁的质量为x,生成的四氧化三铁为y,
 ,
,
![]() 所以y=
所以y=![]()
2.8g-x+![]() =3.44g
=3.44g
x=1.68
剩余的铁为:2.8g-1.68g=1.12g,生成的四氧化三铁为:3.44g-1.12g=2.32g。

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案