题目内容
23、如图1是元素周期表中铝元素的部分信息,如图2是铝原子的结构示意图.下列说法中,不正确的是( )
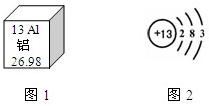

分析:A、根据在原子中,原子序数=质子数=核外电子数,进行解答;
B、根据相对原子质量是有单位的,其单位为“1”,只不过常省略而已,进行解答;
C、根据铝原子的结构示意图即可解答;
D、根据元素的化学性质由最外层电子数 决定,最外层电子数相同的元素化学性质相似,进行解答.
B、根据相对原子质量是有单位的,其单位为“1”,只不过常省略而已,进行解答;
C、根据铝原子的结构示意图即可解答;
D、根据元素的化学性质由最外层电子数 决定,最外层电子数相同的元素化学性质相似,进行解答.
解答:解:A、根据在原子中,原子序数=质子数=核外电子数,元素周期表中铝元素的信息可知:铝原子的质子数为13;故A正确;
B、根据相对原子质量是有单位的,其单位为“1”,只不过常省略而已,所以铝的相对原子质量为26.98;故B错误;
C、根据铝原子的结构示意图可知:铝原子的核外电子分三层排布;故C正确;
D、根据元素的化学性质由最外层电子数 决定,所以说铝元素的化学性质与铝原子的最外层电子数有密切的关系;故D正确;
故选B.
B、根据相对原子质量是有单位的,其单位为“1”,只不过常省略而已,所以铝的相对原子质量为26.98;故B错误;
C、根据铝原子的结构示意图可知:铝原子的核外电子分三层排布;故C正确;
D、根据元素的化学性质由最外层电子数 决定,所以说铝元素的化学性质与铝原子的最外层电子数有密切的关系;故D正确;
故选B.
点评:本题考查学生对在原子中,原子序数=质子数=核外电子数和元素的化学性质由最外层电子数 决定及相对原子质量的单位的知识理解与掌握,并能在解题中灵活应用.

练习册系列答案
 应用题点拨系列答案
应用题点拨系列答案 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
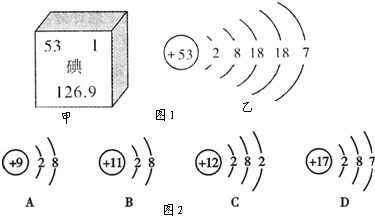 随着日本福岛核电站放射性碘泄漏,碘这种元素被人们所认知.如图1是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图.
随着日本福岛核电站放射性碘泄漏,碘这种元素被人们所认知.如图1是元素周期表中提供的碘元素的部分信息及碘原子的结构示意图. ”和“
”和“ ”分别表示质子数不同的两种原子,则下列图中表示化合物的是
”分别表示质子数不同的两种原子,则下列图中表示化合物的是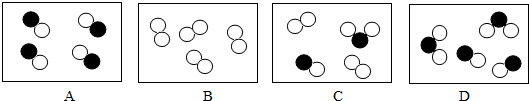

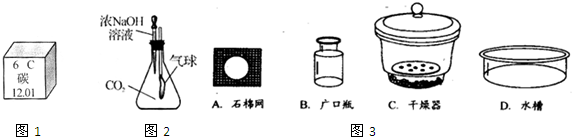
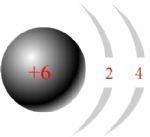
 碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.
碳是形成化合物种类最多的元素,含碳物质是中学化学研究的重要内容.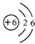 D.碳的相对原子质量为12.01
D.碳的相对原子质量为12.01