题目内容
课本中“‘复分解反应发生条件’的活动与探究”用到H2SO4、Ba(NO3)2、NaOH、K2CO3四种溶液.某校化学兴趣小组的同学对实验后的废液进行了探究.
取废液少许,测得其pH为12.
[提出问题]:废液中除含OH-外,还含有哪些离子呢?
[理论分析]:废液是由四种盐混合而成的.这四种盐电离出的8种离子(H+、SO42-、Ba2+、NO3-、Na+、OH-、K+、CO32-)之间会相互发生反应.废液的pH为12,显碱性,所以一定不存在的一种离子是________;有三种离子在任何条件下都会存在,它们是NO3-、K+和________.
[猜想与假设]:甲同学:另外,可能还含有SO42-、CO32-
乙同学:另外,可能还含有Ba2+
丙同学:另外,可能还含有Ba2+、SO42-、CO32-
以上甲、乙、丙三位同学的假设中,________同学的假设一定不成立,原因是________.
[实验验证]:选择其中一种可能成立的假设,设计实验进行验证.我选择________同学的假设,实验方案如下:
| 实验步骤 | 实验现象 | 结论 |
________ | ________ | ________ |
②继续加稀盐酸直到无气体冒出;
③③再滴加氯化钡溶液,观察现象 有气泡冒出
有白色沉淀产生 废液中有CO32-
废液中有SO42-
甲同学的假设成立
分析:[理论分析]:因为溶液显碱性,所以溶液中一定含有较多的OH-,根据复分解反应发生的条件即可分析出溶液中一定不存在H+;因为所有的硝酸盐、钠盐、钾盐均可溶于水,根据复分解反应发生的条件即可分析出答案;
[猜想与假设]:根据Ba2+可以与SO42-和CO32-反应,即可知丙不正确;
[实验验证]:根据SO42-和CO32-的检验方法去分析:CO32-可以与酸反应放出气体,SO42-与Ba2+反应生成白色沉淀.
解答:【理论分析】因为溶液显碱性,所以溶液中一定有OH-,根据复分解反应发生的条件,H+与OH-会发生反应,即两者不共存,所以溶液中一定不含H+;
因为所有的硝酸盐、钠盐、钾盐都可溶于水,根据复分解反应发生的条件,所以NO3-、K+、Na+这三种离子无论什么条件下都会存在.
故答案为:H+、Na+
【猜想与假设】因为硫酸钡、碳酸钡是沉淀,所以Ba2+与SO42-和CO32-不能共存.
故答案为:丙、Ba2+与SO42-和CO32-不能共存
【实验验证】我选择甲同学的假设,用下面的方法即可验证SO42-、CO32-.
取溶液少许,向溶液中加入稀盐酸,若有无色无味的气体冒出就可以说明溶液中有CO32-;继续加稀盐酸直到无气体冒出,然后向溶液中滴加氯化钡溶液,若有白色沉淀产生则证明溶液中也含SO42-.
故答案为:甲
| 实验步骤 | 现象 | 结论 |
| ①取少量废液于试管中,向其中滴加稀盐酸; ②继续加稀盐酸直到无气体冒出; ③③再滴加氯化钡溶液,观察现象 | 有气泡冒出 有白色沉淀产生 | 废液中有CO32- 废液中有SO42- 甲同学的假设成立 |
点评:检验混合溶液中的几种离子时,一定要注意排除其他离子的干扰,即确定了一种离子后,在验证下一种离子之前要除完全前一种离子,以免引起干扰.

⑴【提出问题】发生复分解反应应具备哪些条件?
⑵【活动探究】该小组同学进行以下四组实验,发现均能反应,请写出④的化学方程式:
①硝酸钡溶液与稀硫酸 ②稀硫酸与碳酸钾溶液 ③稀盐酸与氢氧化钠溶液
④硝酸钡溶液与碳酸钾溶液: 。
⑶【理论分析】上述反应为什么能够发生?是因为在这些反应物的溶液中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水。如:
①中有Ba 2+ + SO42- → BaSO4↓ ②中有H + + CO32- → H2O + CO2↑
③中有H + + OH- → H2O ④中有 两种离子,所以才发生化学反应。
⑷【得出结论】经过分析,该小组同学得出以下结论:生成物中是否有沉淀或气体或水,是判断酸、碱、盐之间能否发生复分解反应的主要条件。
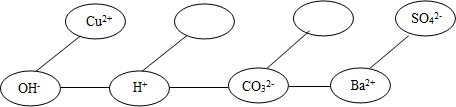
⑸【形成网络】按照一定的顺序排列某些离子,就可以形成一种知识网络。在网络中,用“——”相连接的阴、阳离子间能两两结合生成沉淀或气体或水。
 现有Ca 2+、HCO3- 两种离子,请将它们填入下面合适的“ ”内,使其形成一个更为完整的复分解反应的知识网络。
现有Ca 2+、HCO3- 两种离子,请将它们填入下面合适的“ ”内,使其形成一个更为完整的复分解反应的知识网络。
⑹【拓展应用】根据得出的结论解决以下问题:
| 物质 | 在溶剂A 中溶解度 | 在溶剂B 中溶解度 |
| AgNO3 | 170 | 86 |
| Ba(NO3)2 | 9.3 | 97.2 |
| AgCl | 1.5×10-4 | 0.8 |
| BaCl2 | 33.3 | 约为0 |
某校化学兴趣小组的同学学习了酸、碱、盐的知识后,对课本中“酸、碱、盐之间并不是都能发生复分解反应”这句话产生了兴趣,展开了探究性学习。
⑴【提出问题】发生复分解反应应具备哪些条件?
⑵【活动探究】该小组同学进行以下四组实验,发现均能反应,请写出④的化学方程式:
①硝酸钡溶液与稀硫酸 ②稀硫酸与碳酸钾溶液 ③稀盐酸与氢氧化钠溶液
④硝酸钡溶液与碳酸钾溶液: 。
⑶【理论分析】上述反应为什么能够发生?是因为在这些反应物的溶液中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水。如:
①中有Ba 2+ + SO42- → BaSO4↓ ②中有H + + CO32- → H2O + CO2↑
③中有H + + OH- → H2O ④中有 两种离子,所以才发生化学反应。
⑷【得出结论】经过分析,该小组同学得出以下结论:生成物中是否有沉淀或气体或水,是判断酸、碱、盐之间能否发生复分解反应的主要条件。
⑸【形成网络】按照一定的顺序排列某些离子,就可以形成一种知识网络。在网络中,用“——”相连接的阴、阳离子间能两两结合生成沉淀或气体或水。
 现有Ca
2+、HCO3- 两种离子,请将它们填入下面合适的“
”内,使其形成一个更为完整的复分解反应的知识网络。
现有Ca
2+、HCO3- 两种离子,请将它们填入下面合适的“
”内,使其形成一个更为完整的复分解反应的知识网络。

⑹【拓展应用】根据得出的结论解决以下问题:
|
物质 |
在溶剂A 中溶解度 |
在溶剂B 中溶解度 |
|
AgNO3 |
170 |
86 |
|
Ba(NO3)2 |
9.3 |
97.2 |
|
AgCl |
1.5×10-4 |
0.8 |
|
BaCl2 |
33.3 |
约为0 |
已知t℃时四种化合物在溶剂A和溶剂B中各自的溶解度(g/100 g溶剂)如右表所示。t℃时表中四种化合物在溶剂A中发生复分解反应的化学方程式为:BaCl2 + 2 AgNO3 == 2 AgCl↓ + Ba(NO3)2则表中四种化合物中某两种化合物在溶剂B中能发生复分解反应的化学方程式为: 。
某校化学兴趣小组的同学学习了酸、碱、盐的知识后,对课本中“酸、碱、盐之间并不是都能发生复分解反应”这句话产生了兴趣,展开了探究性学习.
(1)【提出问题】发生复分解反应应具备哪些条件?
(2)【活动探究】该小组同学进行以下四组实验,发现均能反应,写出反应④的化学方程式:
①硝酸钡溶液与稀硫酸 ②稀硫酸与碳酸钾溶液 ③稀盐酸与氢氧化钠溶液 ④硝酸钡溶液与碳酸钾溶液:______.
(3)【理论分析】上述反应未什么能够发生?是因为在这些反应物的溶液中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水.如:
①中有Ba2++SO42-→BaSO4↓ ②中有H++CO32-→H2O+CO2↑ ③中有H++OH-→H2O ④中有______两种离子,所以才发生化学反应.
(4)【得出结论】经过分析,该小组同学得出以下结论:生成物中是否有沉淀或气体或水,是判断酸、碱、盐之间能否发生复分解反应的主要条件.
(5)【形成网络】按照一定的顺序排列某些离子,就可以形成一种知识网络.在网络中,用“--”相连接的阴、阳离子间能两两结合生成沉淀或气体或水.现有Ca2+、HCO3-两种离子,请将它们填入下面合适的“ ”内,使其形成一个更为完整的复分解反应的知识网络.
”内,使其形成一个更为完整的复分解反应的知识网络.

(6)【拓展应用】根据得出的结论,解决以下问题:
已知t℃时四种化合物在溶剂A和溶剂B中各自的溶解度(g/100g溶剂)如下表所示.
| 物质 | 在溶剂A中的溶解度 | 在溶剂B中的溶解度 |
| AgNO3 | 170 | 86 |
| Ba(NO3)2 | 9.3 | 97.2 |
| AgCl | 1.5×10-4 | 0.8 |
| BaCl2 | 33.3 | 约为0 |
则表中四种化合物中某两种化合物在溶剂B中能发生复分解反应的化学方程式为:______.
(1)【提出问题】发生复分解反应应具备哪些条件?
(2)【活动探究】该小组同学进行以下四组实验,发现均能反应,写出反应④的化学方程式:
①硝酸钡溶液与稀硫酸 ②稀硫酸与碳酸钾溶液 ③稀盐酸与氢氧化钠溶液 ④硝酸钡溶液与碳酸钾溶液:______.
(3)【理论分析】上述反应未什么能够发生?是因为在这些反应物的溶液中有特殊的阴、阳离子,它们两两结合生成了沉淀或气体或水.如:
①中有Ba2++SO42-→BaSO4↓ ②中有H++CO32-→H2O+CO2↑ ③中有H++OH-→H2O ④中有______两种离子,所以才发生化学反应.
(4)【得出结论】经过分析,该小组同学得出以下结论:生成物中是否有沉淀或气体或水,是判断酸、碱、盐之间能否发生复分解反应的主要条件.
(5)【形成网络】按照一定的顺序排列某些离子,就可以形成一种知识网络.在网络中,用“--”相连接的阴、阳离子间能两两结合生成沉淀或气体或水.现有Ca2+、HCO3-两种离子,请将它们填入下面合适的“
 ”内,使其形成一个更为完整的复分解反应的知识网络.
”内,使其形成一个更为完整的复分解反应的知识网络.
(6)【拓展应用】根据得出的结论,解决以下问题:
已知t℃时四种化合物在溶剂A和溶剂B中各自的溶解度(g/100g溶剂)如下表所示.
| 物质 | 在溶剂A中的溶解度 | 在溶剂B中的溶解度 |
| AgNO3 | 170 | 86 |
| Ba(NO3)2 | 9.3 | 97.2 |
| AgCl | 1.5×10-4 | 0.8 |
| BaCl2 | 33.3 | 约为0 |
则表中四种化合物中某两种化合物在溶剂B中能发生复分解反应的化学方程式为:______.
 ”内,使其形成一个更为完整的复分解反应的知识网络.
”内,使其形成一个更为完整的复分解反应的知识网络.