题目内容
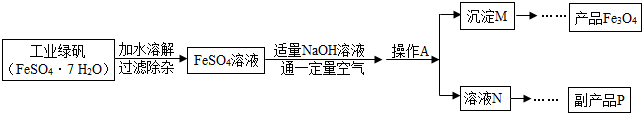
下图是氧化沉淀法生产复印用高档Fe3O4粉的部分工艺流程简图.
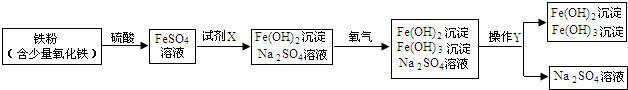
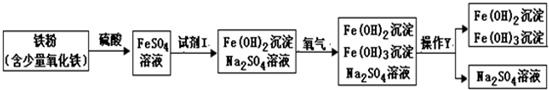
(1)试剂I和操作Y的名称分别为________、________.
(2)硫酸与氧化铁的反应为________.
(3)往铁粉(含少量氧化铁)中加入硫酸,除铁、氧化铁与硫酸发生反应外,一定还发生其它反应.作出这种判断的依据是________.
(4)某铁矿主要成分为Fe3O4,利用CO将该物质中铁还原出来的方程式为________.
解:FeSO4与试剂1生成了Fe(OH)2和Na2SO4
所以试剂1为氢氧化钠;
将溶液和沉淀分开的操作是过滤.
硫酸与氧化铁反应:3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;但在反应后却只有FeSO4,可见一定发生了我们并不知道的反应.
CO还原四氧化三铁生成铁和二氧化碳.Fe3O4+4CO 3Fe+4CO2
3Fe+4CO2
故答案为:(1)氢氧化钠、过滤;
(2)3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;
(3)生成物只有FeSO4一种;
(4)Fe3O4+4CO 3Fe+4CO2.
3Fe+4CO2.
分析:由硫酸亚铁转化为氢氧化亚铁和硫酸钠可以得出试剂1为氢氧化钠.将混合物中沉淀和溶液分开的操作是过滤.酸与金属氧化物发生复分解反应.由我们初中知识可知往铁粉(含少量氧化铁)中加入硫酸,铁、氧化铁与硫酸发生反应生成硫酸亚铁和硫酸铁,但生成物中只有硫酸亚铁,可见在里面一定还发生了我们并不知道的其它反应.
点评:由生成物可以判断反应物,同时也可以根据生成物的种类,来判断发生了几个反应,对于我们还没有学过的反应,不能认为不存在.
所以试剂1为氢氧化钠;
将溶液和沉淀分开的操作是过滤.
硫酸与氧化铁反应:3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;但在反应后却只有FeSO4,可见一定发生了我们并不知道的反应.
CO还原四氧化三铁生成铁和二氧化碳.Fe3O4+4CO
 3Fe+4CO2
3Fe+4CO2故答案为:(1)氢氧化钠、过滤;
(2)3H2SO4+Fe2O3=Fe2(SO4)3+3H2O;
(3)生成物只有FeSO4一种;
(4)Fe3O4+4CO
 3Fe+4CO2.
3Fe+4CO2.分析:由硫酸亚铁转化为氢氧化亚铁和硫酸钠可以得出试剂1为氢氧化钠.将混合物中沉淀和溶液分开的操作是过滤.酸与金属氧化物发生复分解反应.由我们初中知识可知往铁粉(含少量氧化铁)中加入硫酸,铁、氧化铁与硫酸发生反应生成硫酸亚铁和硫酸铁,但生成物中只有硫酸亚铁,可见在里面一定还发生了我们并不知道的其它反应.
点评:由生成物可以判断反应物,同时也可以根据生成物的种类,来判断发生了几个反应,对于我们还没有学过的反应,不能认为不存在.

练习册系列答案
相关题目