题目内容
【题目】某补钙剂的有效成分是碳酸钙,其说明书中表明碳酸钙含量是60%.其他成分不含鈣且不与盐酸反应.现取1Og补钙剂进行实验,过程如图所示,试通过计算判断该补钙剂中碳酸钙含量是否与说明书相符? 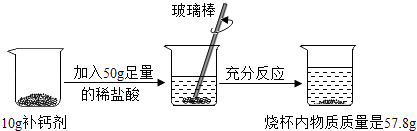
【答案】解:因该反应中只有二氧化碳是气体,由质量守恒定律可知,二氧化碳的质量为10g+50g﹣57.8g=2.2g; 设补钙剂中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+ | CO2↑ |
100 | 44 |
x | 2.2g |
![]()
x=5g
该补钙剂中碳酸钙含量是: ![]() =50%<60%
=50%<60%
答:该补钙剂中钙元素的质量分数与说明书不相符
【解析】由质量守恒定律可知,二氧化碳的质量为10g+50g﹣57.8g=2.2g; 设补钙剂中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+ | CO2↑ |
100 | 44 |
x | 2.2g |
![]()
x=5g
该补钙剂中碳酸钙含量是: ![]() =50%<60%
=50%<60%
先根据质量守恒定律及物质的状态可计算二氧化碳的质量,再利用化学反应方程式来计算碳酸钙的质量,根据碳酸钙中钙的质量来分析该补钙剂中含钙元素的质量分数是否与说明书相符.

练习册系列答案
相关题目
【题目】某同学向过氧化氢溶液中加入二氧化锰制取氧气,相关数据如下:
反应前物质的质量/g | 充分反应后物质的质量/g | |
过氧化氢溶液 | 二氧化锰 | 固体与液体混合物质量 |
68.0 | 0.1 | 66.5 |
请计算:
(1)该同学制得氧气的质量为 .
(2)该同学所用过氧化氢溶液的溶质质量分数.(相对原子质量:H﹣1 O﹣16)