题目内容
有一包不纯的Na2CO3样品,其中只含一种杂质,现取该样品5.3g与足量稀盐酸反应生成2.4g CO2,则所混杂质可能是( )A.BaCO3
B.K2CO3
C.CaCO3
D.MgCO3
【答案】分析:要计算含有的另一种杂质,可以根据归一法求混合物的相对分子质量,之后分析给定物质的相对分子质量
解答:解:设该盐为纯净的+2价碳酸盐,设该金属为M,对应的碳酸盐的相对分子质量为x.
MCO3+2HCl=MCl2+CO2↑+H2O
x 44
5.3g 2.4g
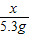 =
=
解得:x≈97;
由于碳酸钠的相对分子质量为106,所以所含杂质的相对分子质量必须小于97,给定物质中只有碳酸镁的相对分子质量为84,小于97.故选D.
故选D.
点评:本题考查了混合碳酸盐与酸反应生成二氧化碳质量,完成此题,需使用极值法和平均值法.
解答:解:设该盐为纯净的+2价碳酸盐,设该金属为M,对应的碳酸盐的相对分子质量为x.
MCO3+2HCl=MCl2+CO2↑+H2O
x 44
5.3g 2.4g
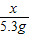 =
=
解得:x≈97;
由于碳酸钠的相对分子质量为106,所以所含杂质的相对分子质量必须小于97,给定物质中只有碳酸镁的相对分子质量为84,小于97.故选D.
故选D.
点评:本题考查了混合碳酸盐与酸反应生成二氧化碳质量,完成此题,需使用极值法和平均值法.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
有一包不纯的Na2CO3样品,其中只含一种杂质,现取该样品5.3g与足量稀盐酸反应生成2.4g CO2,则所混杂质可能是( )
| A、BaCO3 | B、K2CO3 | C、CaCO3 | D、MgCO3 |