题目内容
元素周期表是学习和研究化学的重要工具。请根据下表(元素周期表的部分内容)回答有关问题:
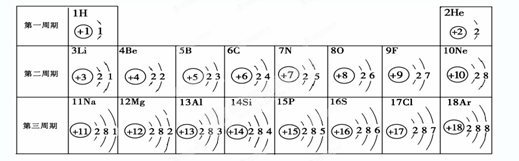
(1)请从上表中查出关于硼元素的一条信息____________。
(2)第3周期(横行)中属于金属元素的是 (填一种),其阳离子是 (填离子符号)
(3)第11号元素与第17号元素组成的物质是 ,构成该物质的微粒是 (选填“分子”、“原子”或“离子”)。
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是 (填标号)。
a.He和Ne b.B和Mg c.Al和Si d.F和Cl
(5)上述元素在周期表中处于同一周期的原因是_______。
(6)研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
(7)第6号碳元素和氢元素形成的物质乙炔在空气中燃烧放出大量热,生成二氧化碳和水,写出该反应的文字表达式

(1)请从上表中查出关于硼元素的一条信息____________。
(2)第3周期(横行)中属于金属元素的是 (填一种),其阳离子是 (填离子符号)
(3)第11号元素与第17号元素组成的物质是 ,构成该物质的微粒是 (选填“分子”、“原子”或“离子”)。
(4)在元素周期表中,同一族(纵行)的元素具有相似的化学性质。则下列各组元素具有相似化学性质的是 (填标号)。
a.He和Ne b.B和Mg c.Al和Si d.F和Cl
(5)上述元素在周期表中处于同一周期的原因是_______。
(6)研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
(7)第6号碳元素和氢元素形成的物质乙炔在空气中燃烧放出大量热,生成二氧化碳和水,写出该反应的文字表达式
(1)硼原子原子核内质子数为5或硼原子核外电子数为5有两个电子层等。
(2)Na Na+
(3)NaCl 离子
(4)a,d
(5)电子层数相同
(6)从左到右,原子半径逐渐减小。
(7)乙炔+氧气 二氧化碳+水
二氧化碳+水
(2)Na Na+
(3)NaCl 离子
(4)a,d
(5)电子层数相同
(6)从左到右,原子半径逐渐减小。
(7)乙炔+氧气
 二氧化碳+水
二氧化碳+水试题分析:从元素周期表中可以看到很多信息,例如原子的核电荷数,质子数,相对原子质量,算出中子数等等,这里只写出一条就行。第三周期的金属有钠Na,镁Mg,铝Al,后面有要求写出其阳离子,则三种金属阳离子分别是Na+ ;Mg 2+; Al 3+ ,写出一种就可以了。第11号元素是Na,其原子最外层电子数是1个,17号元素是氯元素,最外层电子是7个。要形成8电子稳定结构,钠原子失去一个电子,氯原子得到一个电子,形成氯化钠离子化合物,化合物中氯离子与钠离子个数比为1比1,所以化学式为NaCl。在(4)题中,给出信息:在元素周期表中,同一族(纵行)的元素具有相似的化学性质。所以在给出选项中寻找属于表格中同一竖行的就可以了。只是容易再选了a以后漏掉d。仔细观察表格同一周期的元素的原子具有相同的电子层。在(6)中有用信息是:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。依次类推第三周期也是如此。第(7)题 第6号碳元素和氢元素形成的物质乙炔在空气中燃烧放出大量热,生成二氧化碳和水,写出该反应的文字表达式文字表达式只要找出反应物是什么,写在左边,生成物是什么写在右边,中间用向“→”连接即可。

练习册系列答案
相关题目


