题目内容
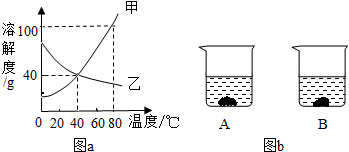
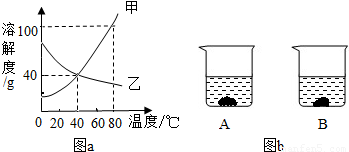
 24、如图,是甲、乙两种固体物质的溶解度曲线,请据此回答(1)(2)(3)的问题.
24、如图,是甲、乙两种固体物质的溶解度曲线,请据此回答(1)(2)(3)的问题.(1)t2℃时,甲的溶解度
大于
乙的溶解度(填“大于”“小于”或“等于”).(2)t1℃时,100g水中溶解20g甲,溶液刚好饱和;那么,50g水中溶解
10
g乙,溶液达到饱和.(3)t1℃时,若要将甲物质的饱和溶液变为不饱和溶液,可采用的方法是
加溶剂(或加水或升温)
.(4)请根据以下表格中的信息回答问题:
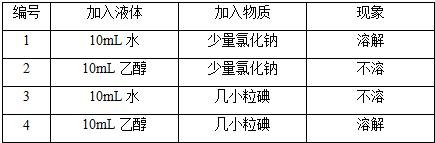
①在同一条件下,物质的溶解能力与溶剂的性质和
溶质的性质
有关.②固体物质的溶解能力除与上述因素有关外,还与外界条件有关.在溶剂种类确定的情况下,要比较硝酸钾和氯化钠的溶解能力,实验中需要控制的因素是
温度、溶剂的量(或溶质的量)
.分析:(1)运用溶解度曲线,比较两种物质在指定温度下溶解度的大小;
(2)分析题中数据,推断t1℃时甲物质的溶解度,然后再运用两种物质溶解度交点的意义推断乙物质此温度下的溶解度;
(3)根据物质的溶解性的特点,把饱和溶液变成不饱和溶液;
(4)通过四组实验结果的对比,探究影响物质溶解性的因素.
(2)分析题中数据,推断t1℃时甲物质的溶解度,然后再运用两种物质溶解度交点的意义推断乙物质此温度下的溶解度;
(3)根据物质的溶解性的特点,把饱和溶液变成不饱和溶液;
(4)通过四组实验结果的对比,探究影响物质溶解性的因素.
解答:解(1)t2℃时,甲物质溶解度曲线处于乙物质的曲线之上,甲物质的溶解度大于乙物质.
故答:大于;
(2)t1℃时,100g水中溶解20g甲,溶液刚好饱和,则可以得知此温度下物质甲的溶解度为20g;
t1℃时乙物质溶解度曲线与甲物质的曲线相交,两物质溶解度相等,所以乙物质溶解度也为20g,100g水溶解乙20g达饱和;
由以上分析可得:t1℃时50g水中溶解乙物质10g达饱和.
故答:10;
(3)由溶解度曲线可知,甲、乙两物质的溶解度都随温度升高而增大,所以通过升高温度和增加溶剂都可以使两物质的饱和溶液变成不饱和溶液.
故答:升温(或加水或加溶剂);
(4)①探究实验1与实验2对比或实验3志实验4对比,可以得出物质的溶解能力与溶剂的性质有关;实验1与实验3或实验2与实验4对比,可以得出物质的溶解能力与溶质的性质有关.
故答:溶质的性质;
②比较硝酸钾和氯化钠的溶解能力,可采取等质量溶剂溶解两种物质至饱和方法,溶解多的物质溶解能力大;也可采取取等质量的两种物质加适量水溶解,刚好完全溶解时需要水的量少的溶解能力大.由于物质溶解会受到温度的影响,所以在进行实验时要在相同温度的水中进行.所以在溶剂种类确定的情况下,还需要控制温度、溶剂的量(或溶质的量).
故答:温度、溶剂的量(或溶质的量).
故答:大于;
(2)t1℃时,100g水中溶解20g甲,溶液刚好饱和,则可以得知此温度下物质甲的溶解度为20g;
t1℃时乙物质溶解度曲线与甲物质的曲线相交,两物质溶解度相等,所以乙物质溶解度也为20g,100g水溶解乙20g达饱和;
由以上分析可得:t1℃时50g水中溶解乙物质10g达饱和.
故答:10;
(3)由溶解度曲线可知,甲、乙两物质的溶解度都随温度升高而增大,所以通过升高温度和增加溶剂都可以使两物质的饱和溶液变成不饱和溶液.
故答:升温(或加水或加溶剂);
(4)①探究实验1与实验2对比或实验3志实验4对比,可以得出物质的溶解能力与溶剂的性质有关;实验1与实验3或实验2与实验4对比,可以得出物质的溶解能力与溶质的性质有关.
故答:溶质的性质;
②比较硝酸钾和氯化钠的溶解能力,可采取等质量溶剂溶解两种物质至饱和方法,溶解多的物质溶解能力大;也可采取取等质量的两种物质加适量水溶解,刚好完全溶解时需要水的量少的溶解能力大.由于物质溶解会受到温度的影响,所以在进行实验时要在相同温度的水中进行.所以在溶剂种类确定的情况下,还需要控制温度、溶剂的量(或溶质的量).
故答:温度、溶剂的量(或溶质的量).
点评:相同条件下,物质溶解的越多,物质的溶解性越大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目