题目内容
【题目】Ⅰ.小茗同学利用硫酸铜溶液进行趣味实验,他将浸泡了硫酸铜溶液的滤纸在酒精灯火焰上点燃,观察到滤纸颜色变白,由湿变干后燃烧,在燃烧后的灰烬中出现了红色固体,他很好奇,进行了相关探究,请填写有关空白.
[实验目的]探究红色固体组成
(1)[查阅资料]
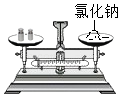
①温度达200℃时,白色CuS04开始分解生成CuO和另一种氧化物,此反应前后各元素化合价保持不变,请写出CuSO4开始分解时的化学方程式 .
②温度超过1000℃时,CuO分解生成Cu2O,Cu2O呈红色,可与稀硫酸反应,化学方程式为:Cu2O+H2SO4═CuSO4+Cu+H2O
(2)[做出猜想]假设红色固体成分:①可能是Cu②可能是Cu2O③还可能是的混合物.
(3)[实验探究及推理]若取少量红色固体于试管中,加入稀硫酸:
①若固体不溶解,溶液仍呈无色,确定红色固体为 , 同时也说明滤纸燃烧时的温度低于℃.
②若固体溶解,溶液呈蓝色,是否可以确定红色固体成分(填“是”或“否”),原因是 .
③Ⅱ.小茗同学又做了氢气还原氧化铜的实验,结果试管内壁上粘有紫红色物质,老师给了一瓶稀盐酸,请问在实验室条件下如何洗净该试管?简述操作过程 .
【答案】
(1)CuSO4![]() CuO+SO3↑
CuO+SO3↑
(2)Cu和Cu2O
(3)铜;1000;否;氧化铜也会与稀硫酸反应;先在空气中加热红色固体,使红色物质变成黑色,然后加入盐酸进行清洗
【解析】I【查阅资料】①硫酸铜在加热的条件下生成氧化铜和三氧化硫,化学方程式为:CuSO4![]() CuO+SO3↑;【做出猜想】温度超过1000℃,CuO才分解生成氧化亚铜(Cu2O);Cu2O呈红色,则CuO的生成物可能为Cu,也可能为Cu2O,还有可能为Cu、Cu2O的混合物;【实验探究及推理】①所设计的实验:向红色固体中加入足量稀硫酸,由于铜不能与稀硫酸发生反应而Cu2O能与稀硫酸反应生成铜和硫酸铜,反应后溶液呈蓝色说明固体中含有Cu2O;若无现象,则固体中只含有铜,所以确定红色固体为铜,同时也说明滤纸燃烧时的温度低于1000℃;②氧化铜、氧化亚铜都会与稀硫酸反应生成硫酸铜溶液,所以不可以确定红色固体成分,原因是:氧化铜也会与稀硫酸反应;II铜不会与稀盐酸反应,氧化铜会与稀盐酸反应,所以操作过程是:先在空气中加热红色固体,使红色物质变成黑色,然后加入盐酸进行清洗. 所以答案是:I【查阅资料】①CuSO4
CuO+SO3↑;【做出猜想】温度超过1000℃,CuO才分解生成氧化亚铜(Cu2O);Cu2O呈红色,则CuO的生成物可能为Cu,也可能为Cu2O,还有可能为Cu、Cu2O的混合物;【实验探究及推理】①所设计的实验:向红色固体中加入足量稀硫酸,由于铜不能与稀硫酸发生反应而Cu2O能与稀硫酸反应生成铜和硫酸铜,反应后溶液呈蓝色说明固体中含有Cu2O;若无现象,则固体中只含有铜,所以确定红色固体为铜,同时也说明滤纸燃烧时的温度低于1000℃;②氧化铜、氧化亚铜都会与稀硫酸反应生成硫酸铜溶液,所以不可以确定红色固体成分,原因是:氧化铜也会与稀硫酸反应;II铜不会与稀盐酸反应,氧化铜会与稀盐酸反应,所以操作过程是:先在空气中加热红色固体,使红色物质变成黑色,然后加入盐酸进行清洗. 所以答案是:I【查阅资料】①CuSO4![]() CuO+SO3↑;
CuO+SO3↑;
【做出猜想】Cu、Cu2O;
【实验探究及推理】①铜,1000;(2)否,氧化铜也会与稀硫酸反应;
II先在空气中加热红色固体,使红色物质变成黑色,然后加入盐酸进行清洗.
【考点精析】利用金属材料的选择依据和书写化学方程式、文字表达式、电离方程式对题目进行判断即可得到答案,需要熟知黑色金属:通常指铁、锰、铬及它们的合金.重金属:如铜、锌、铅等;有色金属轻金属:如钠、镁、铝等;有色金属:通常是指除黑色金属以外的其他金属;注意:a、配平 b、条件 c、箭号.