题目内容
【题目】在“宏观﹣微观﹣符号”之间建立联系,是化学学科特有的思维方式。如图是某反应的微观示意图,下列说法正确的是( )
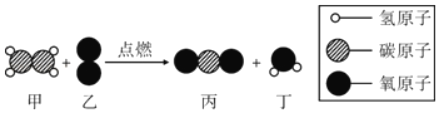
A. 该反应中相对分子质量最大的是甲
B. 参加反应的甲、乙分子个数比为 1:3
C. 反应前后分子的种类和数目都不变
D. 参加反应的甲、乙物质的质量比为 28:32
【答案】B
【解析】
由反应的微观示意图可知,该反应是乙烯燃烧生成二氧化碳和水,反应的化学方程式是:C2H4+3O2![]() 2CO2+2H2O。
2CO2+2H2O。
A、甲的相对分子质量为28;乙的相对分子质量是32,丙的相对分子质量为44,丁的相对分子质量为18,丙的相对分子质量最大,故说法错误;
B、由化学方程式可知,参加反应的甲、乙分子个数比为 1:3,故说法正确;
C、由化学方程式可知,化学反应前后分子的种类发生了变化,故说法错误;
D、由化学方程式可知,参加反应的甲、乙物质的质量比为:28:(32×3)=7:24,故说法错误。
故选:B。

【题目】某校兴趣小组在实验室中完成制取氧气的实验。它们取氯酸钾和二氧化锰的混合物共3.0克放入大试管中加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min | 1.0 | 1.5 | 2.0 | 2.5 | 3.0 |
剩余固体质量/g | 2.55 | 2.25 | 2.10 | 2.04 | 2.04 |
分析表中数据,完成下列问题:
(1)完全反应后,生成氧气多少克。
(2)原混合物中氯酸钾的质量分数是多少?
【题目】某化学兴趣小组为探究金属铝和铜的活动性强弱,开展了以下活动。
(查阅资料)
经查阅,金属铝在常温下能与空气中的氧气反应生成致密的氧化铝薄膜。该反应的化学方程式为_____。
(对比实验)
编号 | 操作 | 现象 |
甲 | 将表面未打磨的铝丝浸入CuSO4溶液中 | 无明显现象 |
乙 | 将表面打磨后的铝丝浸入CuSO4溶液中 | 铝丝表面析出红色固体 |
丙 | 将表面未打磨的铝丝浸入CuCl2溶液中 | 铝丝表面析出红色固体 |
(1)比较实验乙和实验_____(填“甲”或“丙”)可得知:打磨能破坏氧化铝薄膜。
(2)实验乙中反应的化学方程式为_____,据此可知金属活动性Al比Cu_____(填“强”或“弱”)。
(3)小明同学对实验丙的现象进行分析,认为H2O对氧化铝薄膜有破坏作用。但此观点马上被其他同学否定,否定的依据是_____。
(猜测与探究)
小组同学针对实验丙的现象,经讨论后猜测:Cl-破坏了氧化铝薄膜。
为检验此猜测是否正确,他们首先向两支试管中加入相同的CuSO4溶液,并均浸入表面未打磨的铝丝,然后进行了新的探究:
操作 | 现象 | 结论 | 推论 |
(1)向一支试管中再加入 NaCl固体 | 铝丝表面析 出红色固体 | 氧化铝薄膜 被破坏 | Na+或①_____能 破坏氧化铝薄膜 |
(2)向另一支试管中再加入 Na2SO4固体 | ②_____ | 氧化铝薄膜 未被破坏 | Na+和SO42都不能 破坏氧化铝薄膜 |
(结论与反思)
得出结论:前述猜测_____(填“正确”或“不正确”)。总结反思:本次探究充分运用了比较法和控制变量法。