题目内容
为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
| 物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
A.表中a的值为5.6 B.X可能是该反应的催化剂
C.X可能含有氢元素 D.X只含碳元素
A
解析试题分析:A反应前物质的总质量为4.4g+12.8g=17.2g;反应后物质的总质量为7.2g+4.4g+ag。根据反应前后,物质的总质量不变且容器为密闭容器可知:7.2g+4.4g+ag=17.2g。则a=5.6 此项正确。B物质X在反应前的质量为零,反应后的质量为5.6g;应为生成物。此项不正确。C根据质量守恒定律可知:反应前后元素的质量不变。反应前氢元素的质量即丙烷中氢元素的质量为:4.4g ×(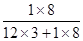 ×100%)=0.8g;反应后水中氢元素的质量为:7.2g×(
×100%)=0.8g;反应后水中氢元素的质量为:7.2g×(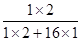 ×100%)="0.8" g;二者相等,所以X中没有氢元素。此项不正确。D根据质量守恒定律可知:反应前后元素的质量不变。反应前碳元素的质量即丙烷中碳元素的质量为:4.4g ×(
×100%)="0.8" g;二者相等,所以X中没有氢元素。此项不正确。D根据质量守恒定律可知:反应前后元素的质量不变。反应前碳元素的质量即丙烷中碳元素的质量为:4.4g ×(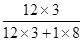 ×100%)=3.6g;反应后水二氧化碳中碳元素的质量为:4.4g×(
×100%)=3.6g;反应后水二氧化碳中碳元素的质量为:4.4g×(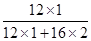 ×100%)="1.2" g;所以X中含碳元素的质量为3.6g—1.2 g="2.4" g<5.6g。因此X中不可能只含碳元素。此项不正确。
×100%)="1.2" g;所以X中含碳元素的质量为3.6g—1.2 g="2.4" g<5.6g。因此X中不可能只含碳元素。此项不正确。
考点:质量守恒定律、根据化学式的计算

高氯酸铵(NH4ClO4)可用作火箭推进剂,其发生分解反应的化学方程式为
2NH4ClO4△N2↑+Cl2↑+4X↑+2O2↑,则X的化学式为
| A.NH3 | B.H2O | C.H2 | D.HCl |
水是生命之源,我们应了解并爱护水资源。下列说法错误的是
| A.自来水厂常用ClO2消毒,ClO2中氯元素的化合价为+2 |
| B.为使水中的悬浮杂质沉降,可在水中加人适量的明矾 |
| C.通过过滤的方法可以将不溶于水的固体杂质与水分离开来 |
| D.5mL水和5mL酒精混合,溶液体积小于10mL,说明分子间有空隙 |
今年央视3.15晚会上曝光了部分涂改液中有毒物质甲苯、二甲苯超标34倍。下列关于甲苯(化学式为C7H8)的分析中,不正确的是
| A.从组成上看:甲苯由碳元素和氢元素组成 |
| B.从变化上看:甲苯完全燃烧生成二氧化碳和水 |
| C.从结构上看:甲苯由7个碳原子和8个氢原子构成 |
| D.从分类上看:甲苯属于有机物 |
实验室中利用过氧化氢、氯酸钾、高锰酸钾都可以制取氧气,其原因是
| A.都属于氧化物 | B.都含有氧气 | C.都含有氧分子 | D.都含有氧元素 |
亚硒酸钠(Na2SeO3)能消除加速人体衰老的活性氧,亚硒酸钠中硒元素(Se)的化合价为
| A.+2 | B.+3 | C.+4 | D.+5 |
对生活中下列现象的解释错误的是 ( )
| | 现 象 | 解 释 |
| A | 湿衣服在夏天比在冬天干得快 | 温度升高,分子运动速率加快 |
| B | 6000L氧气在加压下可装入容积为40L的钢瓶中 | 气体分子间间隔大,易于压缩 |
| C | 在无外力下,花粉会在平静的水面上移动 | 分子在不断运动 |
| D | 自行车轮胎在阳光下暴晒而炸裂 | 分子受热,体积变大 |
氯乙烷(C2H5Cl)是某种镇痛急救药的有效成分.下列说法正确的是( )
| A.氯乙烷中碳、氢元素的质量比为2:5 | B.氯乙烷是一种有机物 |
| C.氯乙烷中氢元素的质量分数最大 | D.氯乙烷由碳原子、氢原子、氯原子构成 |
金属单质M与非金属单质硫发生如下反应为2M + S 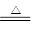 M2S。甲、乙二组学生在实验室分别进行该实验,加入的M和硫的质量各不相同。充分反应后,实验数据记录如下表,则M的相对原子质量是
M2S。甲、乙二组学生在实验室分别进行该实验,加入的M和硫的质量各不相同。充分反应后,实验数据记录如下表,则M的相对原子质量是
| | M的质量/ | S的质量/ g | M2S的质量/ g |
| 甲 | 6.0 | 2.5 | 7.5 |
| 乙 | 7.0 | 1.5 | 7.5 |