题目内容
(2006?淄博)“禽流感”是一种H5N1病毒引起的传染病,从禽类发病到人类染病引起全世界的关注.预防这类病毒的方法是消毒,常见的氧化剂、甲醛、碱类物质等都有较好的杀死病毒的作用.其中NaOH溶液因消毒效果好且廉价易得被广泛使用,从而使工业烧碱用量增加.但工业烧碱中含有杂质碳酸钠,为了测定氢氧化钠的质量分数,某工厂甲、乙两实验员分别设计了如下的实验方案:
Ⅰ甲的实验方案是:准确称量一定质量的烧碱样品于烧杯中加蒸馏水溶解,再加入过量氯化钡溶液至沉淀完全,过滤、洗涤、烘干、称量.
(1)甲实验员洗涤沉淀的具体操作是:向沉淀中加入蒸馏水,然后过滤,重复2~3次.确认沉淀已洗涤干净的依据是
(2)氯化钡溶液和氯化钙溶液都可以与碳酸钠溶液反应生成沉淀,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是
Ⅱ乙的方案如下图所示:
ω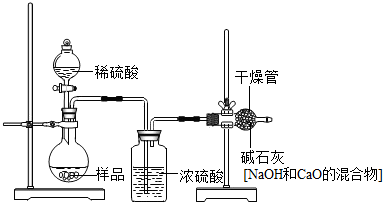
(1)根据乙的实验装置图分析,请你说出浓硫酸的作用是
①装置的气密性不好;②加入的稀硫酸量不足;③干燥管与空气直接相通会吸收空气中的水蒸气和CO2.
(2)经测定知,该工业烧碱中氢氧化钠的质量分数为80%,某养殖户需配制2000g 2%的氢氧化钠溶液对禽舍进行杀菌消毒,需这种工业烧碱
Ⅰ甲的实验方案是:准确称量一定质量的烧碱样品于烧杯中加蒸馏水溶解,再加入过量氯化钡溶液至沉淀完全,过滤、洗涤、烘干、称量.
(1)甲实验员洗涤沉淀的具体操作是:向沉淀中加入蒸馏水,然后过滤,重复2~3次.确认沉淀已洗涤干净的依据是
取适量洗涤后的溶液于试管中,滴加Na2CO3溶液无沉淀产生
取适量洗涤后的溶液于试管中,滴加Na2CO3溶液无沉淀产生
.(2)氯化钡溶液和氯化钙溶液都可以与碳酸钠溶液反应生成沉淀,但使用氯化钡溶液比氯化钙溶液所得的结果具有更高的精确度,原因是
Ca(OH)2微溶于水,使沉淀偏多;等量Na2CO3分别与CaCl2、BaCl2反应生成的BaCO3沉淀质量大,称量时误差小(只要答出一项就得分)
Ca(OH)2微溶于水,使沉淀偏多;等量Na2CO3分别与CaCl2、BaCl2反应生成的BaCO3沉淀质量大,称量时误差小(只要答出一项就得分)
.Ⅱ乙的方案如下图所示:
ω

(1)根据乙的实验装置图分析,请你说出浓硫酸的作用是
吸水
吸水
,碱石灰的作用是吸收生成的CO2
吸收生成的CO2
.按照乙的方案进行测定,将会导致不可避免的误差,例如:装置内空气中的CO2没有排出;反应产生的CO2未被完全吸收.该设计中还有一项也会导致不可避免的误差,你认为应该是下列选项中的(填序号)③
③
.①装置的气密性不好;②加入的稀硫酸量不足;③干燥管与空气直接相通会吸收空气中的水蒸气和CO2.
(2)经测定知,该工业烧碱中氢氧化钠的质量分数为80%,某养殖户需配制2000g 2%的氢氧化钠溶液对禽舍进行杀菌消毒,需这种工业烧碱
50
50
g.分析:I(1)沉淀洗涤干净则洗涤后的溶液中不含有滤液中的溶质,可通过对此物质的检验,判断沉淀洗涤干净;
(2)根据氯化钙、氯化钡与混合溶液反应的不同,分析选择不同试剂对测定结果产生的影响;
II(1)根据物质的性质及连接方式,分析装置图中浓硫酸和碱石灰的作用,并对装置产生的误差进行分析;
(2)根据加水稀释前后溶液中溶质质量不变,计算加水稀释所需要浓溶液的质量.
(2)根据氯化钙、氯化钡与混合溶液反应的不同,分析选择不同试剂对测定结果产生的影响;
II(1)根据物质的性质及连接方式,分析装置图中浓硫酸和碱石灰的作用,并对装置产生的误差进行分析;
(2)根据加水稀释前后溶液中溶质质量不变,计算加水稀释所需要浓溶液的质量.
解答:解:Ⅰ(1)沉淀表面不再沾有滤液则洗涤剂干净,因此可取洗涤沉淀后的溶液,滴加能与氯化钡形成沉淀的碳酸钠溶液,观察是否有沉淀现象,若无沉淀则可说明洗涤干净;
(2)向混合溶液中加入氯化钙,氯化钙与碳酸钠反应生成碳酸钙沉淀,但溶液的大量的OH-与Ca2+能形成微溶于水的Ca(OH)2而使沉淀质量偏大;另外钙元素的相对原子质量小于钡原子相对原子质量,因而生成碳酸钙的质量小于碳酸钡质量,称量精度偏小;
Ⅱ(1)浓硫酸有吸水性,在装置中放置于碱石灰前,防止混在气体中的水分对测定气体二氧化碳产生影响;碱石灰可吸收二氧化碳,因此装置中的碱石灰用来吸收反应产生的二氧化碳;由于装置中不可避免地会存在二氧化碳的残留,因此该装置存在测定不精确的不可避免的误差;而且碱石灰与大气相通,空气中的二氧化碳也会与碱石灰发生反应,从而造成测定误差,此误差因装置关系而无法避免,分析所给的选项可以知道选项③符合刚才的分析,故选③;
(2)设需要这种工业烧碱的质量为x
x?80%=2000g×2%
解得:x=50g
故答案为:Ⅰ(1)取适量洗涤后的溶液于试管中,滴加Na2CO3溶液无沉淀产生.
(2)Ca(OH)2微溶于水,使沉淀偏多;等量Na2CO3分别与CaCl2、BaCl2反应生成的BaCO3沉淀质量大,称量时误差小(只要答出一项就得分);
Ⅱ(1)吸水;吸收生成的CO2;③;
(2)50.
(2)向混合溶液中加入氯化钙,氯化钙与碳酸钠反应生成碳酸钙沉淀,但溶液的大量的OH-与Ca2+能形成微溶于水的Ca(OH)2而使沉淀质量偏大;另外钙元素的相对原子质量小于钡原子相对原子质量,因而生成碳酸钙的质量小于碳酸钡质量,称量精度偏小;
Ⅱ(1)浓硫酸有吸水性,在装置中放置于碱石灰前,防止混在气体中的水分对测定气体二氧化碳产生影响;碱石灰可吸收二氧化碳,因此装置中的碱石灰用来吸收反应产生的二氧化碳;由于装置中不可避免地会存在二氧化碳的残留,因此该装置存在测定不精确的不可避免的误差;而且碱石灰与大气相通,空气中的二氧化碳也会与碱石灰发生反应,从而造成测定误差,此误差因装置关系而无法避免,分析所给的选项可以知道选项③符合刚才的分析,故选③;
(2)设需要这种工业烧碱的质量为x
x?80%=2000g×2%
解得:x=50g
故答案为:Ⅰ(1)取适量洗涤后的溶液于试管中,滴加Na2CO3溶液无沉淀产生.
(2)Ca(OH)2微溶于水,使沉淀偏多;等量Na2CO3分别与CaCl2、BaCl2反应生成的BaCO3沉淀质量大,称量时误差小(只要答出一项就得分);
Ⅱ(1)吸水;吸收生成的CO2;③;
(2)50.
点评:在解此类题时,首先弄懂题意,从大量的叙述中找出有用的,此类题的起点高,但是落点低,答案大都是平时学过的,难度不大.

练习册系列答案
相关题目