题目内容
 29、向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.
29、向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想]①可能有一种气体和另一种物质生成 ②反应过程中可能有能量变化.现利用如图装置进行.
[实验探究]实验一:探究反应后生成的气体是什么?
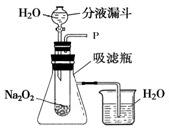
(1)打开右图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃.说明生成的气体是
氧气(或O2)
.(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:
过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生
实验二:继续探究反应后生成的另一种是什么?
(1)小张猜想另一种物质是Na2CO3,小军认为不可能.小军的依据是:
根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3
.
取少量反应后所得的溶液于试管中,加入稀盐酸;没有气泡产生;生成物中没有Na2CO3
为了证实小军的看法,请你设计一个证明CO32-不存在的实验.

(2)小军取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈
碱
性.[表达与交流]由实验探究的结果,写出过氧化钠和水反应的化学方程式
2Na2O2+2H2O═4NaOH+O2↑
.分析:(1)根据氧气的特性进行分析,氧气能使带火星的木条复燃.
(2)可以从导致锥形瓶中气体压强增大的因素去分析.
实验二
(1)根据质量守恒定律,在化学反应前后,元素的种类不会增减.
要验证碳酸钠,需要加入盐酸,看是否有气体产生.
(2)根据碱性溶液能使酚酞变红的性质进行分析,根据实验现象推测生成物进而完成化学方程式.
(2)可以从导致锥形瓶中气体压强增大的因素去分析.
实验二
(1)根据质量守恒定律,在化学反应前后,元素的种类不会增减.
要验证碳酸钠,需要加入盐酸,看是否有气体产生.
(2)根据碱性溶液能使酚酞变红的性质进行分析,根据实验现象推测生成物进而完成化学方程式.
解答:解:实验一
(1)能使带火星的木条复燃的气体只能是氧气,故答案为:氧气.
(2)伸入烧杯中的导管口有气泡冒出,说明锥形瓶中的气体压强增大了,但是又没有新的气体生成,只能是里面的温度升高了,故答案为:过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生.
实验二
(1)根据质量守恒定律,在化学反应前后,元素的种类不会增减,只是原子的重新组合过程.故答案为:根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3.
要验证碳酸钠,需要加入盐酸,看是否有气体产生.故答案为:
(2)碱性溶液能使酚酞变红,过氧化钠可以和水反应生成氢氧化钠和氧气.故答案为:碱,2Na2O2+2H2O═4NaOH+O2↑.
(1)能使带火星的木条复燃的气体只能是氧气,故答案为:氧气.
(2)伸入烧杯中的导管口有气泡冒出,说明锥形瓶中的气体压强增大了,但是又没有新的气体生成,只能是里面的温度升高了,故答案为:过氧化钠与水反应放出热量,使吸滤瓶中的空气受热膨胀,因此伸入烧杯中的导管口看到有气泡产生.
实验二
(1)根据质量守恒定律,在化学反应前后,元素的种类不会增减,只是原子的重新组合过程.故答案为:根据质量守恒定律,反应物中没有碳元素,所以生成物中不可能有Na2CO3.
要验证碳酸钠,需要加入盐酸,看是否有气体产生.故答案为:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量反应后所得的溶液于试管中,加入稀盐酸 | 没有气泡产生 | 生成物中没有Na2CO3 |
点评:本题主要考查了对质量守恒定律的微观理解和过氧化钠与水反应的综合理解,综合性强,难度适中.

练习册系列答案
相关题目

