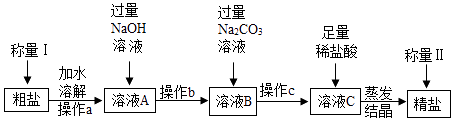
题目内容
【题目】节约能源、保护环境、低碳生活是全社会应该倡导的生活方式. 
(1)下列物质都可以用来作为燃料:①煤;②氢气:③石油;④天然气.其中,最清沽的燃料是(填序号).
(2)充分燃烧1000g天然气和煤所产生的CO2和SO2气体的质量如图所示,根据图示分析,下列说法正确的是 .
A.煤燃烧产生的气体更易导致酸雨
B.该天然气中不含硫元素
C.煤燃烧对环境影响较小
D.煤和天然气的燃烧都有温室气体产生
(3)硫酸型酸雨的形成主要经过以下两步:①SO2在空气中被粉尘催化氧化得到SO3;②SO3与水化合形成硫酸.其中反应①、②的化学方程式为 .
(4)某火力发电厂为了防止环境污染,需将废气中的二氧化硫进行处理,其发生的主要反应为2CaCO3+2SO2+O2=2CaSO4+CO2 , 若100g废气中含有3.2g二氧化硫,则处理500g这种废气需含碳酸钙80%的石灰石g.
【答案】
(1)②
(2)AD
(3)2SO2+O2![]() 2SO3;SO3+H2O═H2SO4
2SO3;SO3+H2O═H2SO4
(4)31.25
【解析】解:(1)煤、石油、天然气、乙醇燃烧都会产生二氧化碳气体,会造成温室效应,氢气燃烧的产物是水,所以答案是:②.(2))A.根据图示可知,煤燃烧产生的二氧化硫的多,更易导致酸雨,故A正确;
B.天然气燃烧生成二氧化硫,所以该天然气中含硫元素,故B错误;
C.根据图示可知,天然气和煤燃烧后都会产生二氧化碳气体,等质量的天然气完全燃烧产生的二氧化硫比等质量的煤完全燃烧产生的二氧化硫少很多,因此燃煤更容易导致 酸雨,对环境影响比较大,故C错误;
D.煤和天然气的燃烧都生成二氧化碳,所以都有温室气体产生,故D正确;
所以答案是:AD;(3)SO2在空气中被粉尘催化氧化得到SO3,反应的化学方程式为:2SO2+O2 ![]() 2SO3.三氧化硫和水反应的化学方程式为:SO3+H2O═H2SO4.(4)设500g废气中二氧化硫的质量是x,则
2SO3.三氧化硫和水反应的化学方程式为:SO3+H2O═H2SO4.(4)设500g废气中二氧化硫的质量是x,则
![]()
x=16g
设处理废气需要含碳酸钙80%的石灰石的质量为y则
2CaCO3+ | 2SO2+O2═2CaSO4+2CO2 |
200 | 128 |
80%y | 16g |
![]()
y=31.25g
答案:(1)②;(2)A、D;(3)2SO2+O2 ![]() 2SO3 SO3+H2O═H2SO4;(4)31.25
2SO3 SO3+H2O═H2SO4;(4)31.25
【考点精析】本题主要考查了书写化学方程式、文字表达式、电离方程式和根据化学反应方程式的计算的相关知识点,需要掌握注意:a、配平 b、条件 c、箭号;各物质间质量比=系数×相对分子质量之比才能正确解答此题.