题目内容
【题目】(1)在KCl和K2CO3 的混合物中,钾元素的质量分数为54%,则该混合物中氯元素的质量分数是:_____________。
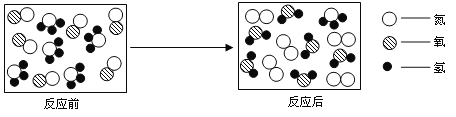
(2)NH3在一定的条件下能跟O2反应,反应过程可用下列示意图表示(注:![]() 表示氮原子,●表示氧原子,O表示氢原子;各物质未配平)。请分析在该反应中参加反应的NH3与O2的分子个数之比为_____________。
表示氮原子,●表示氧原子,O表示氢原子;各物质未配平)。请分析在该反应中参加反应的NH3与O2的分子个数之比为_____________。
![]()
【答案】 28.8% 4∶5
【解析】(1)KCl中钾元素的质量分数=![]() 52.3%;碳酸钾中钾元素的质量分数=
52.3%;碳酸钾中钾元素的质量分数=![]() 56.1%;设镁100g混合物中由氯化钾的质量为x,则:52.3%x+56.1%
56.1%;设镁100g混合物中由氯化钾的质量为x,则:52.3%x+56.1%![]() (100g-x)=100g
(100g-x)=100g![]() 54%,x=60.4g,那么氯元素的质量=60.4g
54%,x=60.4g,那么氯元素的质量=60.4g![]() 28.8g,氯元素的质量分数=
28.8g,氯元素的质量分数=![]() 28.8%;(2)由反应的微观示意图可知该反应的化学方程式表示为4NH3+5O2===4NO+6H2O,故在该反应中参加反应的NH3与O2的分子个数之比为4:5 。
28.8%;(2)由反应的微观示意图可知该反应的化学方程式表示为4NH3+5O2===4NO+6H2O,故在该反应中参加反应的NH3与O2的分子个数之比为4:5 。

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目