题目内容
完成下列反应的化学方程式,并回答有关问题.(1)光合作用:
(2)实验室用高锰酸钾制取氧气:
(3)铝片投入稀盐酸中:
(4)锌片和硫酸铜溶液反应:
| ||
| 叶绿体 |
(2)高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,化学方程式为:2KMnO4
| ||
(3)铝与盐酸反应生成氯化铝和氢气,2Al+6HCl═2AlCl3+3H2↑;反应物是一种单质和一种化合物,生成物是一种单质和另一种化合物,是置换反应.
(4)锌片和硫酸铜反应生成铜和硫酸锌,Zn+CuSO4═ZnSO4↓+Cu; 根据化学方程式,每65份质量的锌能置换出64份质量的铜,故锌的质量减小.
故答案为:
(1)6CO2+6H2O
| ||
| 叶绿体 |
(2)2KMnO4
| ||
(3)2Al+6HCl═2AlCl3+3H2↑;置换反应;
(4)Zn+CuSO4═ZnSO4↓+Cu;减小.

小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:?
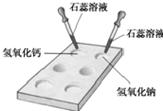
(1) 如右图所示,在白色点滴板上进行实验,请将实验现象填入下表:
|
| 氢氧化钠溶液 | 氢氧化钙溶液 |
| 加紫色石蕊溶液 | 56 | 57 |
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方 程式 58 。?
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式?
59 。?
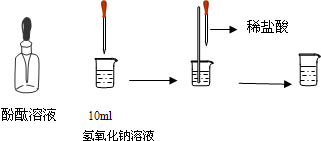
(4)如右图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显 60 色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。这一实验说明:酸与碱作用生成了盐和水,这一反应叫做 61 反应。?
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质。(任写两点)?
① 62
② 63
小黎同学为了进一步加深对“碱的化学性质”的理解,特邀你协助完成下列活动与探究:?
(1) 如右图所示,在白色点滴板上进行实验,请将实验现象填入下表:

|
|
氢氧化钠溶液 |
氢氧化钙溶液 |
|
加紫色石蕊溶液 |
56 |
57 |
(2)回忆检验二氧化碳气体的反应,写出该反应的化学方 程式 58 。?
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式?
59 。?
(4)如右图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显 60 色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。这一实验说明:酸与碱作用生成了盐和水,这一反应叫做 61 反应。?

(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质。(任写两点)?
① 62
② 63
(1)如图所示,在白色点滴板上进行实验,请将实验现象填入下表:
| 氢氧化钠溶液 | 氢氧化钙溶液 | |
| 加紫色石蕊溶液 | ______ | ______ |
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式______.
(4)如图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显______色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止.这一实验说明:酸与碱作用生成了盐和水,这一反应叫做______反应.
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质.(任写两点)?
①______
②______.


(1)如图所示,在白色点滴板上进行实验,请将实验现象填入下表:
| 氢氧化钠溶液 | 氢氧化钙溶液 | |
| 加紫色石蕊溶液 | ______ | ______ |
(3)三氧化硫(SO3)与氢氧化钠反应与上面的反应类似,写出这一反应的化学方程式______.
(4)如图所示,在烧杯中加入10mL氢氧化钠溶液,滴入几滴酚酞试液,溶液显______色,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止.这一实验说明:酸与碱作用生成了盐和水,这一反应叫做______反应.
(5)根据上面的实验和讨论,试归纳出氢氧化钠、氢氧化钙有哪些相似的化学性质.(任写两点)?
①______
②______.