题目内容
取氯酸钾和二氧化锰的混合物26g,加热至固体质量不再减少为止,冷却后称得剩余固体质量为16.4g,将剩余固体加入一定量的足量的水中,充分搅拌后过滤得到10%的氯化钾溶液(假设溶液无损失),请计算:
(1)MnO2的相对分子质量=______。
(2)生成氧气的质量______。
(3)氯化钾溶液中水的质量_____(写出计算过程)。
某石油化工厂化验室的实验员用15%的氢氧化钠溶液洗涤一定量石油产品中的残余硫酸,测得实验数据见下表
实验序号 | 消耗NaOH溶液的质量 | 洗涤后溶液的PH值 |
① | 30g | pH>7 |
② | 40g | pH=7 |
③ | 50g | pH<7 |
请回答下列问题:
(1)计算出一定量石油产品中所含H2SO4的质量,你觉得应该选择实验序号______的数据
(2)若该定量石油产品残余硫酸的质量为100g,计算该残余硫酸的溶质质量分数(写出详细的计算过程)
现有某纯净物X,将其配成无色溶液,取该溶液三等份,分别加入到足量的稀硫酸、澄清石灰水和氯化钠溶液中并振荡,产生的现象如下表。则有关该物质X的描述中正确的是
加入物质 | 稀硫酸 | 澄清石灰水 | 氯化钠溶液 |
实验现象 | 生成气体 | 生成沉淀 | 无明显现象 |
A.物质X中可能含有钾元素
B.物质X的溶液中可能含有SO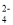
C.物质X可能是碳酸钠
D.物质X一定是化合物
如下图所示,将少量液体 X加入到广口瓶中,关闭活塞,液体 X和固体Y 因发生化学变化而使a侧液柱低于b侧液柱的组合是( )
① | ② | ③ | ④ | |
X | 水 | 水 | 双氧水 | 稀盐酸 |
Y | NH4NO3 | NaOH | MnO2 | Na2CO3 |

A.①②③ B.②③④ C.①② D.③④
某固体混合物可能含有BaCl2、FeCl3、Mg(NO3)2、Na2SO4、CaCO3中的一种或几种,为确定其组成,兴趣小组进行如下探究,请你参与解答相关问题。
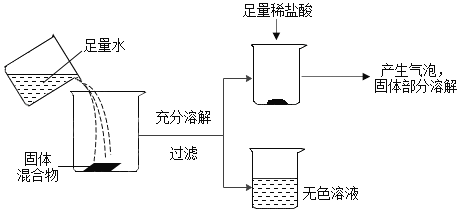
(1)分析图可知,固体混合物中不含有的物质是________。加入水后发生反应的化学方程式为____________
(提出问题)过滤所得无色溶液中含有哪些溶质?
(猜想与假设)猜想无色溶液中所含溶质可能为
猜想I: NaCl、Mg(NO3)2;
猜想II: NaCl、BaCl2;
猜想III: NaCl、Na2SO4;
猜想IV: NaCl、Mg(NO3)2、______
猜想V:含有NaCl、Mg(NO3)2、BaCl2。
(实验探究)
实验操作 | 实验现象 |
①取少量无色溶液于试管中,向其中滴加氢氧化钡溶液 | 产生白色沉淀 |
②在①反应后的试管中,加入足量的稀盐酸 | 白色沉淀部分溶解 |
(结论和反思)
(2)根据探究结果可知,猜想______成立, 步骤②沉淀溶解的化学方程式为_________
(3)若步骤②的现象为“白色沉淀全部溶解”,则该实验探究及步骤设计存在不足,因为这种情况下无法判断猜想_____和猜想_____哪个成立。


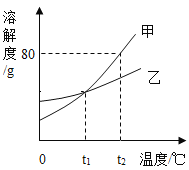

 点燃酒精灯 B.
点燃酒精灯 B.  取用块状固体
取用块状固体 加热液体 D.
加热液体 D.  稀释浓硫酸
稀释浓硫酸