题目内容
【题目】某实验小组将制作皮蛋的原料生石灰、纯碱和食盐放入水中,充分反应后过滤,得到澄清溶液,小亮等几位同学对溶液的成分进行了探究.
(提出问题)溶液中有哪些溶质?
(猜想)以下是三位同学的分析与猜想:

有可能剩余另一种反应物,所以你认为溶液中溶质还可能是_____.
(讨论)你认为小亮、小芳、小红三位同学中谁的猜想不合理,请说明理由._____.
(实验设计)设计实验证明猜想正确.
实验操作 (在短线上填所加试剂的名称) | 预测的现象 | 发生的所有反应的 化学方程式 | 实验结论 |
| _____ | _____ | 小红同学的猜想正确 |
| _____ | _____ | 你的猜想正确 |
(实验分析)小红同学实验中出现了与自己预测的实验现象不一致的情况:她取适量的澄清溶液于试管中,滴入几滴稀盐酸,结果没有气泡产生,于是得出自己的猜想不成立的结论,你是否同意她的判断,请说明理由._____.
【答案】【猜想】有食盐,还有氢氧化钠、氢氧化钙,或NaCl、NaOH、![]() (1分);
(1分);
【讨论】小亮同学的猜想不正确,没有考虑过滤时已将碳酸钙除去(1分)
【实验设计】
实验操作 | 预测的现象 | 发生的所有反应的 | 实验 |
有气泡产生 |
| ||
碳酸钠溶液或二氧化碳气体(1分) | 有白色沉淀产生(1分) |
|
【实验分析】
不同意,因有氢氧化钠存在,滴入几滴稀盐酸量太少,不会立即出现气泡,但Na2CO3有可能存在。(1分)
【解析】
试题【猜想】混合物中的生石灰先与水反应生成氢氧化钙,氢氧化钙再与碳酸钠反应生成氢氧化钠和碳酸钙。氢氧化钠为反应的生成物应存在,食盐没有参与反应应存在;如氢氧化钙过量也可能存在。所以可能是:食盐、氢氧化钠和氢氧化钙。
【讨论】小亮同学的猜想不正确。因为碳酸钙不溶于水,所以在过滤时已将碳酸钙除去。过滤后的溶液中不可能存在碳酸钙。
【实验设计】小红的猜想中含有碳酸钠可与稀盐酸反应生成二氧化碳气体,所以会观察到溶液中有气泡生成。溶液中的氢氧化钠、碳酸钠与盐酸反应的化学方程式为:HCl+NaOH=NaCl+H2O 、Na2CO3+2HCl=2NaCl+H2O+CO2↑
你的猜想正确,则溶液中存在氢氧化钙。所以可能入二氧化碳气体。现象为:溶液变浑浊。反应的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O也可加入碳酸钠溶液。现象为:溶液变浑浊。反应的化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
【实验分析】
不同意,因有溶液中有氢氧化钠存在。当滴入稀盐酸量太少时,发生的是盐酸与氢氧化钠的反应。该反应不生成气泡。应加入足量的盐酸后(把氢氧化钠反应完,再加入)才会出现气泡。

 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案【题目】某学习小组在帮助实验员整理化学试剂时发现了一瓶标签残缺的无色溶液,(如图所示),经实验员分析可知原瓶溶液中的溶质可能是 NaHCO3,NaOH,Na2CO3,NaCl中的一种,请你对该试剂作出猜想并进行实验探究:
(提出问题)这瓶试剂是什么溶液?
(猜想与假设)
甲猜想:NaHCO3溶液
乙猜想:NaOH溶液
丙猜想:Na2CO3溶液
丁猜想:NaCl溶液
(查阅资料)上述四种物质相关信息如下
物质 | NaHCO3 | NaOH | Na2CO3 | NaCl |
常温下溶解度/g | 9.6 | 109 | 21.5 | 36 |
常温下稀溶液的pH | 9 | 13 | 11 | 7 |
(实验探究1)取瓶中溶液少许于试管中,滴加几滴酚酞溶液,溶液变红。
(实验探究2)另取瓶中溶液少许于试管中,滴加足量的稀盐酸,产生生气泡。
(实验分析)通过(实验探究1)可知_____同学的猜想一定错误。
甲同学仔细分析四种物质的相关信息表后发现自已的猜想错误,他的理由是_____。
丙同学分析(实验探究2)并结合以上同学的实验结论,认为原瓶溶液是NaCO3溶液。
(实验探究2)中发生反应的化学方程式为_____。
(讨论质疑)乙认为以上同学分析有漏洞,需要进一步实验确定,于是又进行了如下探究。
(实验探究3)在(实验探究1)试管中的红色溶液中滴加过量氯化钙溶液(中性),充分反应后,试管中溶液仍呈红色,但有白色沉淀产生。
(得出结论)通过(实验探究3)可证明这瓶试剂为_____溶液,但已经部分变质。
(反思与拓展)学习小组反思了这瓶试剂因为_____而变质,得出了该溶液正确的保存方法,若要除去该溶液变质部分所采用的方法是_____(用化学反应方程式表示)。

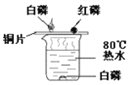
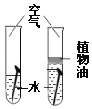
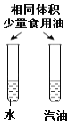
【题目】设计对比实验、控制变量是学习化学的重要方法,下列对比实验不能达到目的( )
编号 | A | B | C | D |
实验 设计 |
|
|
|
|
实验 目的 | 探究温度对分子运动速度的影响 | 探究可燃物燃烧的条件 | 探究铁生锈的条件 | 探究同种物质在不同溶剂中的溶解性 |
A. AB. BC. CD. D