题目内容
 水在实验室和日常生产生活中有很多用途.
水在实验室和日常生产生活中有很多用途.(1)在天然水中有许多杂质,可利用吸附、沉淀、过滤和蒸馏等方法净化,其中净化程度最高的是
(2)从如图所示的实验,可推知水的组成元素是
(3)在用久了的水壶中常会集结着一层厚厚的水垢,这主要是由于自来水中含有的少量Ca(HCO3)2受热发生分解生成碳酸钙、水和二氧化碳的缘故,该反应的化学方程式为
(4)溶液是日常生活中的常见物质,请根据下列各图所示内容回答:
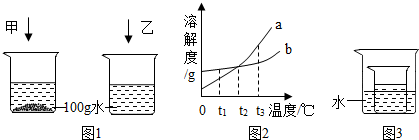
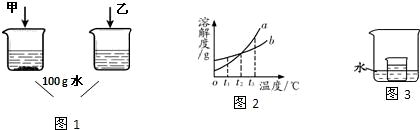
①在t1℃时,等质量的甲和乙两种固体物质在水中的溶解现象如图1所示,要使剩余的固体甲继续溶解可采用的方法是
②若图2中的a、b分别表示甲、乙两种物质的溶解度曲线,乙的曲线是
③在图3所示的实验中,小烧杯内盛放的是t2℃时甲物质的饱和溶液.某同学要使小烧杯内有固体析出时,他向大烧杯的水中可加入下列物质是
A.氧化钙 B.干冰 C.浓硫酸 D.硝酸铵.
分析:(1)常用的净化水的方法有,沉淀、过滤、吸附、蒸馏等,从这几种方法的原理与净化效果分析考虑.
(2)从化学反应的质量守恒定律和元素守恒定律来解答.
(3)可从化学反应的质量守恒定律和元素守恒定律来解答.
(4)可从溶液的性质,溶解度的变化方面分析,考虑做出解答.
(2)从化学反应的质量守恒定律和元素守恒定律来解答.
(3)可从化学反应的质量守恒定律和元素守恒定律来解答.
(4)可从溶液的性质,溶解度的变化方面分析,考虑做出解答.
解答:解:(1)常用的净化水的方法有,沉淀、过滤、吸附、蒸馏等其中只有蒸馏能除去水中所有的杂质,故答案为:蒸馏.
(2)根据化学反应的质量守恒定律和元素守恒定律可推知,产物为氧气和氢气反应物应由氢、氧两种元素组成,故答案为:氢、氧两种元素.
(3)由题知:反应物为Ca(HCO3)2产物为碳酸钙、水和二氧化碳,反应条件为受热,故答案为:Ca(HCO3)2
CaCO3+C02↑+H20
(4)①使溶质继续溶解的方法有:增加溶剂、改变温度等.故答案为:增加溶剂或改变温度.
②由题知在t1℃时,乙的溶解度大于甲可得出乙的曲线是 b.故答案为:b.
③由图2知:甲的溶解度随温度的降低而减小,故加入干冰使温度降低可使甲析出.故答案为:B
(2)根据化学反应的质量守恒定律和元素守恒定律可推知,产物为氧气和氢气反应物应由氢、氧两种元素组成,故答案为:氢、氧两种元素.
(3)由题知:反应物为Ca(HCO3)2产物为碳酸钙、水和二氧化碳,反应条件为受热,故答案为:Ca(HCO3)2
| ||
(4)①使溶质继续溶解的方法有:增加溶剂、改变温度等.故答案为:增加溶剂或改变温度.
②由题知在t1℃时,乙的溶解度大于甲可得出乙的曲线是 b.故答案为:b.
③由图2知:甲的溶解度随温度的降低而减小,故加入干冰使温度降低可使甲析出.故答案为:B
点评:本题考查了水的净化、溶液的性质、溶解度的变化、化学反应的质量守恒定律和元素守恒定律等知识,是一道综合性、实验性较强的题目.

练习册系列答案
相关题目
 水在实验室和日常生产生活中有很多用途.
水在实验室和日常生产生活中有很多用途.