题目内容
某兴趣小组在实验室模拟水厂将浑浊的湘江水净化成自来水,并最终制成蒸馏水,其实验流程如下图所示:

请回答下列问题:
(1)加入明矾的作用是______;操作1的名称是______。
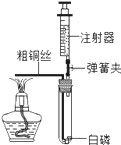
(2)利用如图所示的装置进行操作2,此操作的作用是_____待处理的水应该从____端通入(填“a”或“b”),理由是_________。

(3)取少量的液体D于试管中,滴入肥皂水振荡,发现有较多的浮渣产生,说明此液体为_____(填“软水”或“硬水”),生活中常用_____的方法软化硬水。
(4)通过操作3可以得到净化程度较高的蒸馏水,操作3的名称是____。
练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
下图表示两种气体发生化学反应,其中相同的球代表同种原子。下列说法正确的是

A. 该示意图中有四种分子 B. 该反应表示H2与O2化合生成水
C. 原子在化学反应中不可再分 D. 化学反应前后分子的种类不变
书写下列元素符号
名称 | 符号 | 化合价 | 名称 | 符号 | 化合价 |
钠 | _____ | +1 | 氯 | _____ | ﹣1 |
钙 | _____ | +2 | 氧 | _____ | ﹣2 |
钾 | _____ | +1 | 铵根 | NH4 | +1 |
镁 | _____ | +2 | 硫酸根 | SO4 | ﹣2 |
铝 | _____ | +3 | 氢氧根 | OH | ﹣1 |
铜 | _____ | +2 | 碳酸根 | CO3 | ﹣2 |
铁 | _____ | +2.+3 | 硝酸根 | NO3 | ﹣1 |




 B. 液体取用
B. 液体取用
 D. 滴加液体
D. 滴加液体