题目内容
化学是一门以实验为基础的科学,下面是初中化学中几组重要的对比实验.
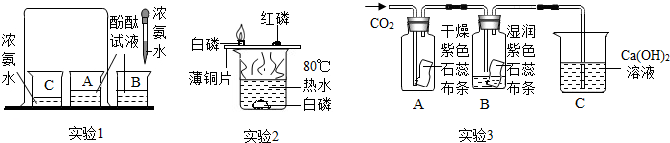
(1)实验1中,观察到A烧杯中的现象是
(2)实验2中,观察到铜片上的白磷燃烧而红磷不燃烧,可得出可燃物燃烧的一个条件为
(3)实验3中,实验过程中布条能变红色的试剂瓶是

(1)实验1中,观察到A烧杯中的现象是
无色变为红色
无色变为红色
,由此可验证分子的性质.(2)实验2中,观察到铜片上的白磷燃烧而红磷不燃烧,可得出可燃物燃烧的一个条件为
温度达到物质的着火点
温度达到物质的着火点
.根据此条件,举一例相关的灭火事例用水灭火
用水灭火
.(3)实验3中,实验过程中布条能变红色的试剂瓶是
B瓶
B瓶
,C烧杯发生反应的化学方程式为CO2+Ca(OH)2═CaCO3↓+H2O
CO2+Ca(OH)2═CaCO3↓+H2O
.分析:(1)从浓氨水呈碱性,易挥发考虑;(2)从物质燃烧的三个条件考虑;(3)根据酸可使紫色石蕊试液变红分析.
解答:解:(1)浓氨水呈碱性,易挥发,说明分子是在不断运动的,挥发的氨水分子进入A,使A中的溶液由无色变为红色;
(2)白磷的着火点是40℃,80℃的热水可使其达到,而红磷的着火点高,热水不能使其达到,说明燃烧的一个条件是:温度达到物质的着火点;用水灭火就是降低了可燃物的温度,使其降到可燃物着火点一下;
(3)二氧化碳遇干燥的紫色石蕊布条不会发生变化,所以A中布条不变色;二氧化碳遇到湿润的紫色石蕊试液布条,首先二氧化碳与水反应生成碳酸,碳酸使石蕊试液布条变成红色;当二氧化碳进入C后,与氢氧化钙溶液反应生成白色沉淀碳酸钙,C中溶液变浑浊.反应物是二氧化碳和氢氧化钙写在等号的左边,生成物是碳酸钙和水写在等号的右边,碳酸钙后面标上沉淀符号;
故答案为:(1)无色变为红色;(2)温度达到物质的着火点;用水把火扑灭(合理给分);(3)B瓶;CO2+Ca(OH)2═CaCO3↓+H2O.
(2)白磷的着火点是40℃,80℃的热水可使其达到,而红磷的着火点高,热水不能使其达到,说明燃烧的一个条件是:温度达到物质的着火点;用水灭火就是降低了可燃物的温度,使其降到可燃物着火点一下;
(3)二氧化碳遇干燥的紫色石蕊布条不会发生变化,所以A中布条不变色;二氧化碳遇到湿润的紫色石蕊试液布条,首先二氧化碳与水反应生成碳酸,碳酸使石蕊试液布条变成红色;当二氧化碳进入C后,与氢氧化钙溶液反应生成白色沉淀碳酸钙,C中溶液变浑浊.反应物是二氧化碳和氢氧化钙写在等号的左边,生成物是碳酸钙和水写在等号的右边,碳酸钙后面标上沉淀符号;
故答案为:(1)无色变为红色;(2)温度达到物质的着火点;用水把火扑灭(合理给分);(3)B瓶;CO2+Ca(OH)2═CaCO3↓+H2O.
点评:本题主要考查燃烧的条件、分子的性质、二氧化碳的性质,考查知识面广,有一定的难度.

练习册系列答案
 核心素养学练评系列答案
核心素养学练评系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案
相关题目
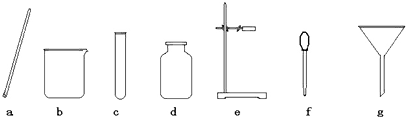
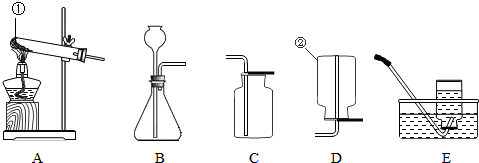
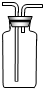
 20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答:
20、化学是一门以实验为基础的科学,规范的实验操作是实验成功的前提,请回答: