题目内容
【题目】膨松剂是一种食品添加剂。它在面包制作过程中发生反应产生气体,使面包变得松软。膨松剂反应产生气体的量作为检验膨松剂品质的一项重要指标。已知某膨松剂含碳酸氢钠、碳酸氢铵中的一种或两种,化学兴趣小组对该膨松剂进行如下探究:
【查阅资料】(1)2NaHCO3 △ Na2CO3+H2O+CO2↑
NH4HCO3 △ NH3↑+H2O+CO2↑
(2)碱石灰的成分是CaO和NaOH
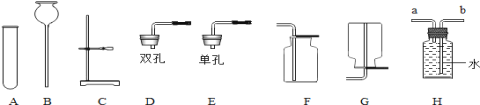
探究Ⅰ:检验膨松剂的成分在玻璃管中加入该膨松剂,按下图连接好装置。

【观察与分析Ⅰ】 点燃酒精灯。
(1)关闭铁夹2,打开铁夹1,观察澄清石灰水变浑浊,说明产物中有二氧化碳,该反应的
化学方程式为 。
(2)打开铁夹2,关闭铁夹1,观察到的现象是 , 说明产物中有氨气。
(3)充分加热后,玻璃管中 (填“有”或“无”)固体。
【实验结论】 该膨松剂的成分是碳酸氢钠和碳酸氢铵混合物。
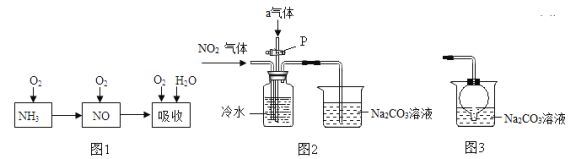
探究Ⅱ:测定膨松剂受热产生气体的质量
用下图装置测定该膨松剂中样品产生的二氧化碳和氨气的质量(装置B装有膨松剂,整套装置气密性良好,各装置中气体吸收剂足量)。

【观察与分析Ⅱ】
(4)通过测定实验前后装置D的质量,其质量差即为样品产生二氧化碳的质量,装置C的作用是 ,装置D的作用是 ,若没有装置E,造成测定结果 (填“偏大”、“不变”或“偏小”)。
(5)实验过程中必须向装置内通入空气,装置A的作用是除去空气中的 (填名称)。
在停止加热后,继续通入空气一段时间,目的是 。
(6)若对装置C、D、E连接顺序进行调整,即可用于测定另一份同质量相同样品受热分解产生氨气的质量。C、D、E连接顺序为 ,通过测定实验前后装置C的质量,其质量差即为样品产生氨气的质量。
【拓展研究】(7)若将产生的氨气通过灼热的氧化铜会生成红色固体、无色液体和气体单质三种物质,则该反应的化学方程式为 。
【答案】(1)Ca(OH)2+CO2=CaCO3↓+H2O (2) 无色酚酞试液变红 (3)有
(4) 除去氨气和水蒸气 吸收二氧化碳 偏大 (5)二氧化碳
将装置中残留的CO2全部鼓入D中或使得生成的CO2全部被D中的碱石灰吸收
(6) DCE (7)2NH3+3CuO△3Cu+3H2O+N2
【解析】
试题分析:(1) 二氧化碳使澄清石灰水变浑浊的化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O
(2)氨气溶于水生成氨水,显碱性,能使无色酚酞试液变红
(3)因为碳酸氢钠加热后会生成碳酸钠固体,故充分加热后,玻璃管中有固体
(4)浓硫酸具有吸水性,能吸收水分,且显酸性,能与氨气反应,故装置C的作用是除去氨气和水蒸气; 装置D的作用是:吸收生成的二氧化碳;若没有装置E,空气中的二氧化碳或水蒸气可能进入到装置E中,从而造成测定结果偏大
(5) 实验过程中必须向装置内通入空气,装置A的作用是除去空气中的二氧化碳,以免空气中的二氧化碳进入到装置E中,从而使结果偏大;在停止加热后,继续通入空气一段时间,目的是:将装置中残留的CO2全部鼓入D中或使得生成的CO2全部被D中的碱石灰吸收
(6)要测定样品受热分解产生氨气的质量,应利用装置C在反应前后质量的变化,但氨气在进入装置C之前,应先用装置D将气体中的水分吸收掉,故C、D、E连接顺序为:DCE
(7) 若将产生的氨气通过灼热的氧化铜会生成红色固体、无色液体和气体单质三种物质,根据质量守恒定律:化学反应前后,元素的种类不变,故红色固体为单质铜,无色液体为水,气体单质为氮气,故该反应的化学方程式为:2NH3+3CuO△3Cu+3H2O+N2

【题目】只用下列鉴别方法不能把待鉴别的物质区分开的是
选项 | 待鉴别的物质 | 鉴别方法 |
A | 二氧化碳和氮气 | 分别向其中伸入燃着的木条,观察燃烧情况 |
B | 硬水和软水 | 加肥皂水,振荡,观察产生泡沫情况 |
C | 过氧化氢溶液和水 | 加二氧化锰,观察有无气泡产生 |
D | 氧气和空气 | 分别向其中伸入燃着的木条,观察燃烧情况 |
【题目】下列各组物质能按照关系图![]() (“→”表示反应一步完成)相互转化的是( )
(“→”表示反应一步完成)相互转化的是( )
X | Y | Z | |
A | Cu | CuO | Cu(OH)2 |
B | Ca(OH)2 | Ca(NO3)2 | CaCl2 |
C | Fe2O3 | Fe | FeSO4 |
D | Na2CO3 | NaOH | Na2SO4 |
【题目】下列有关物质的鉴别、检验、除杂所用的试剂或方法正确的是( )
选项 | 实验目的 | 所用试剂或方法 |
A | 鉴别氯化钠溶液和稀盐酸 | 无色酚酞 |
B | 鉴别硫酸钠溶液和硝酸钾溶液 | 氯化钡溶液 |
C | 除去氧化钙中的少量碳酸钙 | 加水溶解后过滤 |
D | 除去二氧化碳中的HCl | 氢氧化钠溶液 |