题目内容
在化学反应2A+B2=2C中,已知20gA和足量B2充分反应后,生成30g C.已知B2的相对分子质量为32,则C的相对分子质量是( )
A.20 B.32 C.48 D.96
C
解析试题分析:根据质量守恒定律可知20gA和B2充分反应生成30gC时参加反应的B2质量应为30g﹣20g=10g;
设C的相对分子质量是x,则
2A+B2=2C
32 2x
10g 30g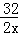 =
=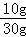
解得x=48.
故选C.
考点:根据化学反应方程式的计算.
点评:此题是对化学方程式计算的考查,解题的关键是把质量守恒定律的内容和化学方程式结合起来进行分析、判断.

练习册系列答案
相关题目
硅在日常生活中的应用十分广泛,下列有关硅说法正确的是( )
| A.硅是地壳中含量最高的金属元素 |
| B.硅原子的相对原子质量为28.06g |
| C.硅的原子序数为14 |
| D.在化学反应中,硅原子容易失去电子 |
下列关于化学反应xA + yB =" mC" + nD(x、y、m、n为化学计量数)的说法中,一定正确的是:
| A.x + y =" m" + n |
| B.若生成物中有水,该反应是中和反应 |
| C.参加反应的A和B的质量比等于生成物C和D的质量比 |
| D.若A和B的质量都为a g,充分反应后生成物的总质量小于或等于2a g |
在一定条件下,在一个密闭容器内发生某反应,测得反应过程中各物质的质量如下表所示,下列说法不正确的是( )
| 物质 | X | Y | Z | W |
| 反应前质量/g | 10 | 3 | 90 | 0 |
| 反应后质量/g | 3.2 | 3 | 待测 | 3.2 |
A.W可能是单质
B.Y可能是催化剂
C.该反应是分解反应
D.反应后Z物质的质量为86.4g
工业用盐亚硝酸钠(NaNO2)有毒,NaNO2中氮元素的化合价为( )
| A.+2 | B.+3 | C.+4 | D.+5 |
过度使用氮肥,是造成土壤和水体污染的一个重要原因.硝酸铵(NH4NO3)是一种常用的氮肥,其中氮元素的化合价是( )
| A.﹣3和+5 | B.+2和+2 | C.﹣5和+3 | D.﹣1和+5 |
下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
A.用过氧化氢溶液和二氧化锰制氧气 2H202 2H20+02↑分解反应 2H20+02↑分解反应 |
B.用天然气作燃料 CH4+202 C02+2H20氧化反应 C02+2H20氧化反应 |
| C.用铁制容器盛放稀盐酸 Fe+2HCl═FeCl2+H2↓置换反应 |
| D.用熟石灰制生石灰 CaO+H20═Ca(OH)2化合反应 |
饮料中的果味大多来自酯类.丁酸乙酯(C6H12O2)是无色具有菠萝香味的液体,常用作食品、饮料的调香剂.关于丁酸乙酯说法正确的是( )
| A.相对分子质量为116g |
| B.由20个原子构成 |
| C.分子中碳、氢、氧原子的个数比为3:6:2 |
| D.氢元素质量分数最小 |
下列有关“2CO+O2 2CO2”的质量关系,不正确的是( )
2CO2”的质量关系,不正确的是( )
| A.若56g CO参加反应,则消耗O2的质量一定是32g |
| B.若16g O2参加反应,则生成CO2的质量一定是44g |
| C.若10g CO2生成,则消耗CO和O2的质量总和一定是10g |
| D.若5g CO和2g O2混合点燃,则CO2生成的质量一定是7g |