题目内容
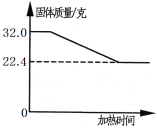
【题目】称取—定质量的氯酸钾和二氧化锰,混合后放人大试管中加热至质量不再变化为止。实验测得固体混合物质量随加热时间变化的相关数据如图所示。为了分离回收二氧化锰和氯化钾,他们在反应后的固体混合物中加入85.1g水,使其中的氯化钾完全溶解,然后通过过滤使二氧化锰与液体分离。请计算:
(1)原混合物中氯酸钾的质量分数?
(2)得到的滤液中氯化钾的质量分数(二氧化锰在水中难溶) ?
【答案】(1)76.6% (2)14.9%
【解析】
试题分析:解:设原混合物中含氯酸钾质量为X,反应后产生氯化钾质量为Y。
由题图可知反应中生成的氧气质量为(32.0g-22.4g)=9.6g
2KClO3![]() 2KCl+3O2↑
2KCl+3O2↑
245 149 96
X Y 9.6g
245∶96= X∶9.6g
X=245×9.6g/96=24.5g
原混合物中氯酸钾的质量分数24.5g/32.0g×100%≈76.6%
149∶96=Y∶9.6g
Y=149×9.6g/96=14.9g
得到的滤液中氯化钾的质量分数14.9g/(14.9g+85.1g) ×100%=14.9%
答:原混合物中氯酸钾的质量分数76.6%;得到的滤液中氯化钾的质量分数14.9%

练习册系列答案
相关题目