题目内容
【题目】根据下列五种微粒的结构示意图,回答下列问题:
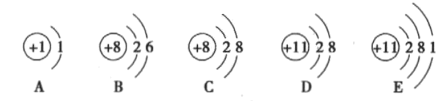
(1)写出A2B2在一定条件下分解的化学反应方程式_________________;
(2)图中这几种元素共同组成化合物的化学式为_______________;
(3)图中的阳离子是(用离子符号表示)_______________;
(4)图中同种元素的微粒是_______________。
【答案】![]() NaOH Na+ B、C或 D、E
NaOH Na+ B、C或 D、E
【解析】
(1)质子数决定元素的种类。A是氢元素,B是氧元素,二者组成的A2B2型化合物是过氧化氢,在二氧化锰的催化作用下,过氧化氢会分解为水和氧气;化学方程式为:2H2O2 ![]() 2H2O+O2↑;
2H2O+O2↑;
(2)A的核电荷数为1,是氢元素,BC的核电荷数为8,是氧元素,DE的核电荷数为11,是钠元素,三种元素组成的化合物是氢氧化钠;故填:NaOH;
(3)同一原子中,质子数=核外电子数=核电荷数=原子序数;在阳离子中:质子数>核外电子;在阴离子中:质子数<核外电子,所以D是带有一个单位正电荷的钠离子—Na+;故填:Na+;
(4)元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),故B与C属于同一种元素、D与E为同一种元素;故填:B、C(或D、E)。

 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】硫酸铜晶体常用于杀虫、杀菌,用废铜料(含少量铁)生产硫酸铜晶体的流程如图所示,请回答下列问题.
![]()
(1)操作 a 的名称是_____;
(2)废铜料中加入足量试剂 X 的目的是_____;
(3)黑色固体 B 与试剂 X 的反应化学方程式是______;
(4)盛放硫酸铜溶液不宜用铁制容器的原因是(用化学方程式解释)______;
(5)根据硫酸铜的溶解度表格所示,最后硫酸铜溶液可以通过蒸发浓缩、_____,过滤、洗涤、干燥的方法得到硫酸铜晶体。
0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 60℃ | 80℃ | 100℃ | |
硫酸铜/g | 23.1 | 27.5 | 32 | 37.8 | 44.6 | 61.8 | 83.8 | 114 |