题目内容
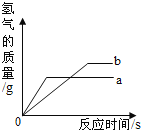
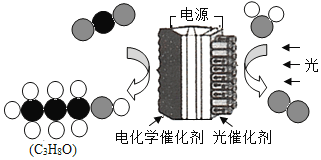
【题目】在一定条件下,将一定质量的A与48g B按如图所示充分反应,当B反应完全时,生成44gC和36gD,则下列说法错误的是( )
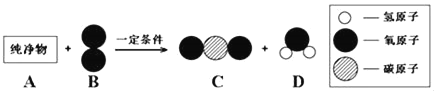
A. 图中所示四种物质均含氧元素
B. 生成C与D的化学计量数之比为1:1
C. 该反应前后原子数目不变
D. 物质A中碳元素的质量分数为37.5%
【答案】B
【解析】
由质量守恒定律可知,参加反应的A物质的质量是:44g+36g﹣48g=32g。A中一定含有碳元素和氢元素,A含有碳元素的质量为![]() ,A含有氢元素的质量为
,A含有氢元素的质量为
![]() ,A中氧元素的质量为
,A中氧元素的质量为![]() ,A中碳、氢、氧原子个数比为
,A中碳、氢、氧原子个数比为
![]() ,故A的化学式为
,故A的化学式为![]() ,所以反应的化学方程式为
,所以反应的化学方程式为
 。
。
A、反应的化学方程式为 ,图中所示四种物质均含氧元素,故A正确;
,图中所示四种物质均含氧元素,故A正确;
B、由方程式可知,生成C与D的化学计量数之比为![]() ,故B不正确;
,故B不正确;
C、由微粒的变化可知,该反应前后原子数目不变,故C正确;
D、物质A中碳元素的质量分数为![]() ,故D正确。故选B。
,故D正确。故选B。

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案 浙江新课程三维目标测评课时特训系列答案
浙江新课程三维目标测评课时特训系列答案
相关题目
【题目】在一个密闭容器中放入W、G、H、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,关于此反应的认识不正确的是( )
物质 | W | G | H | P |
反应前质量/g | 20 | 2 | 1 | 37 |
反应后质量/g | a | 32 | 1 | 12 |
A.a=15
B.H可能是该反应的催化剂
C.若W和P的化学式量之比为1:5,则W和P的化学计量数之比为1:1
D.在反应中,G、P的质量比为5:6