题目内容
实验室中通常用锌和稀硫酸反应生成氢气和硫酸锌(ZnSO4).实验室制取0.4克氢气,需要多少克锌?
解:设需要锌的质量为x.
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.4g
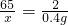
解之得:x=13g.
答:需要锌的质量为13g;
分析:根据锌和稀硫酸反应的化学方程式和制取氢气的质量,列出比例式,即可计算出需要锌的质量.
点评:此题是根据化学方程式的计算题,该题比较简单,就是用一种生成物的质量求一种反应物的质量,属于最基本类型的计算题.
Zn+H2SO4=ZnSO4+H2↑
65 2
x 0.4g
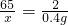
解之得:x=13g.
答:需要锌的质量为13g;
分析:根据锌和稀硫酸反应的化学方程式和制取氢气的质量,列出比例式,即可计算出需要锌的质量.
点评:此题是根据化学方程式的计算题,该题比较简单,就是用一种生成物的质量求一种反应物的质量,属于最基本类型的计算题.

练习册系列答案
相关题目