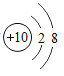
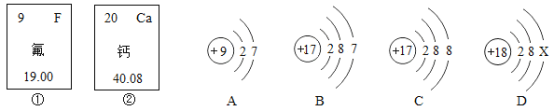
题目内容
【题目】现有31.6克,高锰酸钾加热一段时间后得到固体30.8克,请计算;
(1)生成氧气的质量为多少克_________?
(2)参加反应的高锰酸钾质量为多少克_________?
(3)剩余固体中锰元素的质量分数,计算结果精确到0.1%_________。
【答案】0.8g 7.9g 8.9%
【解析】
(1)根据质量守恒定律可得,生成的氧气的质量为31.6g-30.8g=0.8g;
(2)设分解的高锰酸钾的质量为x,
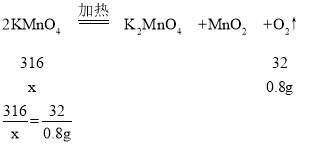
x=7.9g
答:参加反应的高锰酸钾质量为7.9g;
(3)根据质量守恒定量可知,反应前后的元素的质量不变,高锰酸钾中锰元素的质量为7.9g× ![]() ×100%=2.75g,
×100%=2.75g,
剩余固体中锰元素的质量分数为:![]() ×100%
×100%![]() 8.9%
8.9%
答:剩余固体中锰元素的质量分数8.9%。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目