题目内容
(6分)张南同学想测定赤铁矿中氧化铁的质量分数,做法如下,请回答下列问题。
(1)配制稀硫酸。
①配制200g 19.6%的稀硫酸,需要98%的浓硫酸的体积是 ;

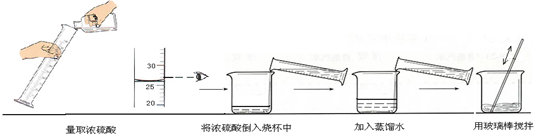
②下图实验过程中出现操作的错误是 。

(2)将赤铁矿粉末,用稀硫酸溶解,反应的化学方程式是 ;
(3)取20g的赤铁矿粉末恰好与l50g的19.6%的稀硫酸完全反应,求解生成硫酸铁质量(x)的比例式为 ;
(4)此赤铁矿中氧化铁的质量分数为 ;
(5)向反应后所得溶液中加入34g水,则所得溶液溶质的质量分数是
【答案】
(1)① 26mL ②读数的方式错误;浓硫酸和水加入的顺序颠倒。
(2)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
(3)294/400=29.4g/x
(4)80%
(5)20%
【解析】略

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目