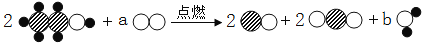题目内容
某化学兴趣小组设计如下实验探究FeCl3溶液的相关性质。
相关信息:Fe和Fe3O4,易被磁铁吸引,FeO是一种黑色固体,不能被磁铁吸引;Fe3O4能与盐酸反应,生成盐和水。FeCl3具有氧化性,与单质铁等物质化合时铁元素化合价会降低。
(1)实验一:将饱和FeCl3溶液在蒸发皿中加热至沸腾后,发现逐渐产生红褐色沉淀,加热时,FeCl3,易与水反应生成红褐色固体物质和盐酸,红色固体的化学式是_______________。
(2)实验二:将实验一蒸发获得的红色固体灼烧,颜色由红色变为红棕色。该反应的化学方程式是__________。
①氢氧化镁,氢氧化铜等物质加热也能分解得到对应的金属氧化物,而氢氧化钠、氢氧化钙等物质则无此性质。结合实验,从物质类别及其溶解性推断,通过加热分解___________可生成对应的金属氧化物。
②将氢氧化镁和铜粉混合物充分加热,得到的固体物质与原混合物质量相同,请问,氢氧化镁和铜粉的质量比为________。
(3)实验三:小组同学用多根玻璃棒蘸取饱和FeCl3溶液于酒精灯火焰上灼烧,在1分钟内观察到玻璃棒表面颜色的变化依次为:黄色、红褐色、红棕色,黑色。
①同学们对黑色物质的成分产生了疑问。联系酒精的可燃性、还原性等相关性质,对黑色物质的成分提出了猜想,经讨论,可能是_______和Fe3O4四种物质中的一种或几种。
②为了确定黑色物质的成分,收集黑色物质,进行了如下实验:
实验步骤 | 实验现象 | 实验结论 |
取黑色粉末用磁铁吸引,观察现象 | 黑色粉末全部被磁铁吸引 | 综合实验现象判断,此黑色物质成分是_______ |
向装有黑色粉末的试管中加入足量的盐酸,充分反应,观察现象 | 固体逐渐溶解,但无气泡产生 |
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案在学习了金属的知识后,同学们开展了有关金属活动性及相关反应的探究。请回答下列问题。
(探究一)小丽提供了一份不完整的金属活动顺序表,如下

金属①具有很好的抗腐蚀性,其原因是_________________。
(探究二):镍(Ni)是一种银白色金属,常用于电镀。小刚为比较镍、铁、银三种金属活动性进行了如下探究。
(猜想与假设)结合金属活动顺序表,小刚作出如下猜想。
猜想一:镍>铁>银
猜想二:________
猜想三:铁>银>镍
(实验验证)实验方案如下。请将表格内容填写完整。
设计实验 | 实验现象 | 结论 | |
实验1 | _________________________ | 镍片上有细小 的气泡生成 | 在金属活动顺序表中,镍位于H之前 |
实验2 | 将铁片加入到NiSO4溶液中 | 铁片上有松散的固体生成 | ______________ |
(实验结论)得出了三种金属的活动性顺序
(探究三):小聪同学将锌和银的混合粉末加入到一定量的硫酸铜溶液中,充分反应后,对所得混合物进行了探究。
(1)写出反应的化学方程式_______________。
(2)小聪欲将充分反应后的固、液混合物进行分离,他采取的操作是________________。
(3)取分离后所得的固体于试管中,加入适量的稀盐酸,有气泡产生,则分离所得固体中含有的物质是___________。
下列物质的用途与性质对应关系不正确的是
选项 | 物质 | 用途 | 性质 |
A | 氮气 | 作保护气 | 常温下,氮气的性质比较稳定 |
B | 一氧化碳 | 冶炼金属 | 一氧化碳具有还原性 |
C | 烧碱固体 | 作气体干燥剂 | 烧碱固体具有吸水性 |
D | 小苏打 | 治疗胃酸过多 | 能与胃酸发生中和反应 |
A.A B.B C.C D.D


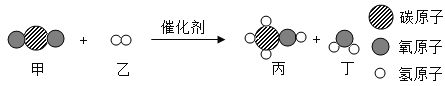
 ”表示碳原子、“
”表示碳原子、“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子)
”表示氧原子)