题目内容
(2004?扬州)已知:(1)等温等压下,等体积的任何气体均具有相同数目的分子数.(2)反应中气体体积的测定均在同温同压下进行.(3)假设每步反应均完全.

则:(1)步骤①说明混合气中一定含有
(2)该混合气中含有的CO的体积是

则:(1)步骤①说明混合气中一定含有
H2O
H2O
,步骤②说明混合气中一定含有CO2
CO2
.混合气中一定不含有的气体是H2
H2
最后剩余的气体的是N2
N2
.(2)该混合气中含有的CO的体积是
50
50
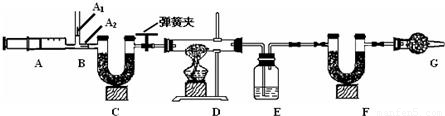
mL.分析:(1)通过分析现象回答问题:无水硫酸铜白色粉末变蓝说明有水生成,碱石灰能吸收二氧化碳,通过灼热氧化铜黑色粉末变红说明具有还原性气体,氮气不与装置中的物质反应.
(2)根据题干信息和各步骤剩余的气体进行计算.
(2)根据题干信息和各步骤剩余的气体进行计算.
解答:解:(1)第一次通过无水硫酸铜变蓝说明含有水蒸气,通过碱石灰气体减少10mL说明混合气体中有二氧化碳气体,通过氧化铜,氧化铜变红说明含有还原性气体,再通入无水硫酸铜不变蓝说明没有水生成,混合气体中不含氢气,含有一氧化碳,再通过碱石灰吸收掉二氧化碳,最后剩余的是氮气.
(2)通过分析,混合气体中含有氮气是20mL,第②步中剩余的70mL气体是一氧化碳和氮气的混合气体,故一氧化碳的体积为50mL.
故答案为:(1)H2O; CO2; H2; N2.
(2)50
(2)通过分析,混合气体中含有氮气是20mL,第②步中剩余的70mL气体是一氧化碳和氮气的混合气体,故一氧化碳的体积为50mL.
故答案为:(1)H2O; CO2; H2; N2.
(2)50
点评:判断气体成分时要注意在反应中是否生成了新的气体,从而准确判断最后得到的气体.

练习册系列答案
相关题目
 Na2CO3↑+CO2↑+H2O
Na2CO3↑+CO2↑+H2O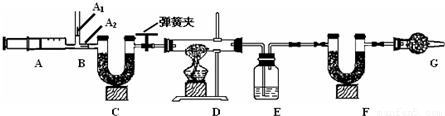
 Na2CO3↑+CO2↑+H2O
Na2CO3↑+CO2↑+H2O