题目内容
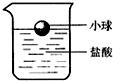
谋研究性学习小组的同学做了如下的实验:将一个不与盐酸反应的小球放入盛有盐酸的烧杯中,小球漂浮于液面,位置如图.将从废电池外壳收集来的锌片放入杯中,该学生观察到的现象是 ;当杯中的盐酸完全反应后,此时小球所处位置与原来相比 (“不变”、“上浮”或“下沉”),其依据是 .
【答案】分析:根据锌片与盐酸反应后溶液的溶质的相对分子质量的改变,推出溶液密度的变化,即溶质相对分子质量越大,溶液密度越大,溶质相对分子质量越小,溶液密度越小;根据浮力公式,溶液密度越大,小球所受浮力越大,小球会向上运动,溶液密度越小,小球所受浮力越小,小球会向下运动.
解答:解:锌的金属活动性在H前,因此可与酸反应生成H2;当锌与稀盐酸反应后,溶液中的溶质发生了改变,由HCl变成了ZnCl2,其相对分子质量增大了,根据ρ= ,在体积没有明显改变的情况下,溶液密度ρ也相应增大;而根据浮力F=ρvg,溶液对小球的浮力变大,因此小球会向上运动.
,在体积没有明显改变的情况下,溶液密度ρ也相应增大;而根据浮力F=ρvg,溶液对小球的浮力变大,因此小球会向上运动.
故答案为:锌逐渐减少,表面有气泡产生,放热、上浮、锌与盐酸反应 溶液密度增大F=pgv排,v排减小,小球上浮.
点评:同学们要学会判断化学反应后溶液中溶质的判断,并根据其相对分子质量的变化判断出溶液密度的变化.
解答:解:锌的金属活动性在H前,因此可与酸反应生成H2;当锌与稀盐酸反应后,溶液中的溶质发生了改变,由HCl变成了ZnCl2,其相对分子质量增大了,根据ρ=
 ,在体积没有明显改变的情况下,溶液密度ρ也相应增大;而根据浮力F=ρvg,溶液对小球的浮力变大,因此小球会向上运动.
,在体积没有明显改变的情况下,溶液密度ρ也相应增大;而根据浮力F=ρvg,溶液对小球的浮力变大,因此小球会向上运动.故答案为:锌逐渐减少,表面有气泡产生,放热、上浮、锌与盐酸反应 溶液密度增大F=pgv排,v排减小,小球上浮.
点评:同学们要学会判断化学反应后溶液中溶质的判断,并根据其相对分子质量的变化判断出溶液密度的变化.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
 谋研究性学习小组的同学做了如下的实验:将一个不与盐酸反应的小球放入盛有盐酸的烧杯中,小球漂浮于液面,位置如图.将从废电池外壳收集来的锌片放入杯中,该学生观察到的现象是
谋研究性学习小组的同学做了如下的实验:将一个不与盐酸反应的小球放入盛有盐酸的烧杯中,小球漂浮于液面,位置如图.将从废电池外壳收集来的锌片放入杯中,该学生观察到的现象是