题目内容
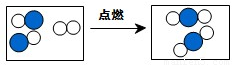
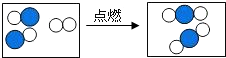
 (1)如图形象地表示了某化学反应前后分子的变化.其中“
(1)如图形象地表示了某化学反应前后分子的变化.其中“ ”表示原子序数为8的原子,“
”表示原子序数为8的原子,“ ”表示原子序数为6的原子,则该反应的化学方程式为:
”表示原子序数为6的原子,则该反应的化学方程式为:2CO+O2
2CO2
| ||
2CO+O2
2CO2
;
| ||
(2)用化学方程式表示铝制品抗腐蚀的原因:
4Al+3O2=2Al2O3
4Al+3O2=2Al2O3
.分析:(1)依据原子序数为8的原子为氧原子,原子序数为6的原子为碳原子,由图中可知,每2个一氧化碳分子和1个氧分子反应生成2个二氧化碳分子.然后根据反应物和生成物及其质量守恒定律可以正确的书写化学方程式;
(2)金属铝能在空气中与氧气反应形成一层致密的保护层,防止铝进一步与氧气发生反应,致使铝制品不易被腐蚀;
(2)金属铝能在空气中与氧气反应形成一层致密的保护层,防止铝进一步与氧气发生反应,致使铝制品不易被腐蚀;
解答:解:(1)原子序数为8的原子为氧原子,原子序数为6的原子为碳原子,由图中信息可知,在化学变化中,一氧化碳分子分解成碳原子和氧原子,氧分子分解成氧原子,每1个碳原子和2个氧原子结合成1个二氧化碳分子.这样一氧化碳和氧气反应就生成二氧化碳,反应的化学方程式为:2CO+O2
2CO2.
(2)铝活动性较强,在常温下即能与氧气发生反应,在铝表面形成一层致密的氧化铝薄膜隔绝铝与氧气的接触,反应的化学方程式为4Al+3O2=2Al2O3;
故答案为:(1)2CO+O2
2CO2;(2)4Al+3O2=2Al2O3;
| ||
(2)铝活动性较强,在常温下即能与氧气发生反应,在铝表面形成一层致密的氧化铝薄膜隔绝铝与氧气的接触,反应的化学方程式为4Al+3O2=2Al2O3;
故答案为:(1)2CO+O2
| ||
点评:解答本题的关键是要掌握化学方程式的书写方法和分子与原子在化学变化中的关系等方面的知识,只有这样才能对问题做出正确的判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
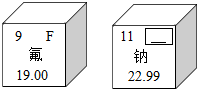 元素周期表是学习和研究化学的重要工具,根据下列信息回答问题:
元素周期表是学习和研究化学的重要工具,根据下列信息回答问题:(1)右图是两种元素在元素周期表中的信息,其中方框的横线上填的是
(2)下表是部分元素的原子结构示意图、主要化合价等信息
| 第二周期 | Li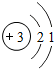 |
Be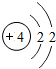 |
B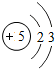 |
C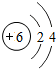 |
N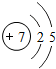 |
O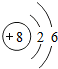 |
F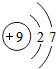 |
| 主要 化合价 |
+1 | +2 | +3 | +4,-4 | +5,-3 | -2 | -1 |
| 第三周期 | Na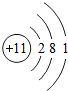 |
Mg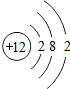 |
Al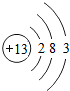 |
Si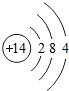 |
P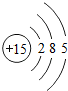 |
S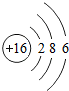 |
Cl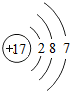 |
| 主要 化合价 |
+1 | +2 | +3 | +4,-4 | +5,-3 | +6,-2 | +7,-1 |
②写出由原子序数为12和17的元素组成化合物的化学式
③上表中各元素的最高正化合价与原子最外层电子数的关系是
④如图形象地表示了某化学反应前后分子的变化.其中“○”表示原子序数为8的原子,“●”表示原子序数为6的原子,则该反应的化学方程式为:
 ”“
”“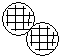 ”“
”“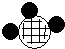 ”分别表示A、B、C三种不同的分子.该反应的化学方程式中A、B、C前的化学计量数之比为
”分别表示A、B、C三种不同的分子.该反应的化学方程式中A、B、C前的化学计量数之比为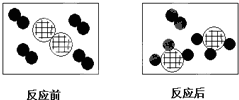
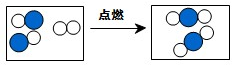 (1)如图形象地表示了某化学反应前后分子的变化.其中“
(1)如图形象地表示了某化学反应前后分子的变化.其中“ ”表示原子序数为8的原子,“
”表示原子序数为8的原子,“ ”表示原子序数为6的原子,则该反应的化学方程式为:______;
”表示原子序数为6的原子,则该反应的化学方程式为:______; ”表示原子序数为8的原子,“
”表示原子序数为8的原子,“ ”表示原子序数为6的原子,则该反应的化学方程式为:______ 2CO2
”表示原子序数为6的原子,则该反应的化学方程式为:______ 2CO2