题目内容
(2002?天津)乙醇是以高粱、玉米、薯类等为原料,经发酵、蒸馏而制得,属于可再生能源.在汽油中加入适量乙醇作为汽油燃料,可节省石油资源,减少汽车尾气的污染.2001年4月2日国家技术监督局发布《车用乙醇汽油》国家标准,并于同年4月15日开始实施.乙醇______完全燃烧时生成CO2和H2O.如果氧气不充足,乙醇燃烧可能还有CO生成.现用以下装置进行实验,确证乙醇燃烧产物中有CO、CO2和H2O.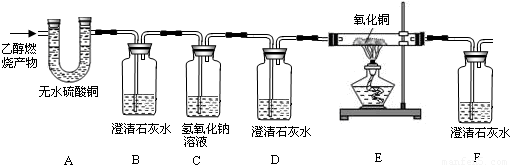
请回答下列问题:
(1)能确证产物中有H2O的现象是______;能确证产物中有CO的现象是______、______.
(2)实验时,可观察到装置B中石灰水变浑浊,D中石灰水无变化.B装置的作用是______;C装置的作用是______;D装置的作用是______.
(3)若乙醇燃烧产物中CO和CO2的总质量为25.2g,其中碳元素与氧元素的质量比为2:5,则参加反应的乙醇的质量为______g,产物中H2O的质量为______g.
(4)科学家发现海底埋藏着大量的“可燃冰”--甲烷的水合物.质量相等的甲烷和乙醇在氧气充足的条件下完全燃烧,产生CO2的质量较多的是______.
【答案】分析:(1)根据白色的无水硫酸铜粉末与水反应生成蓝色的五水硫酸铜回答前一问;根据一氧化碳的还原性和二氧化碳能使澄清的石灰水变浑的性质回答后两问.
(2)根据二氧化碳能使澄清的石灰水变浑及实验验证的过程和要求回答.
(3)根据CO和CO2的总质量为25.2g,其中碳元素与氧元素的质量比为2:5,求出碳元素的质量,再根据乙醇中碳的质量分数求乙醇的质量,最后根据乙醇中氢元素的质量与水中氢元素的质量相等和水中氢元素的质量分数求水的质量.
(4)根据甲烷和乙醇燃烧的化学方程式计算或根据碳元素反应前后质量不变,由二者的含碳量进行判断.
解答:解:(1)白色的无水硫酸铜粉末与水反应生成蓝色的五水硫酸铜,如产物中有H2O生成,则A中的无水硫酸铜由白色变为蓝色;
一氧化碳有还原性,能把黑色的氧化铜还原成红色的铜,同时本身被氧化成二氧化碳,二氧化碳能使澄清的石灰水变浑,所以如是一氧化碳的话,现象应为的玻璃管中黑色的氧化铜变为红色,F中的澄清石灰水变浑浊.
(2)证明二氧化碳存在,可根据二氧化碳能使澄清的石灰水变浑的性质,B装置的作用是验证产物中CO2的存在;
一氧化碳的检验涉及与氧化铜反应生成二氧化碳,故工检验一氧化碳需先除去二氧化碳,再检验是否又生成了新的二氧化碳,所以C装置的作用是除去CO2;D装置的作用是 检验CO2是否已除尽.
(3)CO和CO2的总质量为25.2g,其中碳元素与氧元素的质量比为2:5,碳元素的总质量为25.2g× =7.2g,则乙醇中碳元素的质量也是7.2g,乙醇中碳的质量分数为
=7.2g,则乙醇中碳元素的质量也是7.2g,乙醇中碳的质量分数为 ×100%=52.17%,乙醇的质量为7.2g÷52.17%=13.8g,乙醇中氢元素的质量为13.8g×
×100%=52.17%,乙醇的质量为7.2g÷52.17%=13.8g,乙醇中氢元素的质量为13.8g×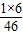 ×100%=1.8g,则生成水中的氢元素也是1.8g,所以水的质量为1.8g÷
×100%=1.8g,则生成水中的氢元素也是1.8g,所以水的质量为1.8g÷ =16.2g.
=16.2g.
(4)甲烷和乙醇在燃烧时,它们中的碳都形成二氧化碳了,二者含碳量越高,产生二氧化碳的质量也越大,甲烷中碳碳的质量占 ,乙醇中碳的质量占
,乙醇中碳的质量占 ,所以产生CO2的质量较多的是甲烷.
,所以产生CO2的质量较多的是甲烷.
故答案为:(1)A中的无水硫酸铜由白色变为蓝色;E的玻璃管中黑色的氧化铜变为红色,F中的澄清石灰水变浑浊;
(2)验证产物中CO2的存在;除去CO2;检验CO2是否已除尽;
(3)13.8;16.2;
(4)甲烷.
点评:能源、信息、材料、环境是当今世界四大首要问题,在能源危机日趋严重的今天,新能源的开发和利用,它既是社会热点,也是化学考查的热点,特别是氢能、乙醇汽油等.
(2)根据二氧化碳能使澄清的石灰水变浑及实验验证的过程和要求回答.
(3)根据CO和CO2的总质量为25.2g,其中碳元素与氧元素的质量比为2:5,求出碳元素的质量,再根据乙醇中碳的质量分数求乙醇的质量,最后根据乙醇中氢元素的质量与水中氢元素的质量相等和水中氢元素的质量分数求水的质量.
(4)根据甲烷和乙醇燃烧的化学方程式计算或根据碳元素反应前后质量不变,由二者的含碳量进行判断.
解答:解:(1)白色的无水硫酸铜粉末与水反应生成蓝色的五水硫酸铜,如产物中有H2O生成,则A中的无水硫酸铜由白色变为蓝色;
一氧化碳有还原性,能把黑色的氧化铜还原成红色的铜,同时本身被氧化成二氧化碳,二氧化碳能使澄清的石灰水变浑,所以如是一氧化碳的话,现象应为的玻璃管中黑色的氧化铜变为红色,F中的澄清石灰水变浑浊.
(2)证明二氧化碳存在,可根据二氧化碳能使澄清的石灰水变浑的性质,B装置的作用是验证产物中CO2的存在;
一氧化碳的检验涉及与氧化铜反应生成二氧化碳,故工检验一氧化碳需先除去二氧化碳,再检验是否又生成了新的二氧化碳,所以C装置的作用是除去CO2;D装置的作用是 检验CO2是否已除尽.
(3)CO和CO2的总质量为25.2g,其中碳元素与氧元素的质量比为2:5,碳元素的总质量为25.2g×
 =7.2g,则乙醇中碳元素的质量也是7.2g,乙醇中碳的质量分数为
=7.2g,则乙醇中碳元素的质量也是7.2g,乙醇中碳的质量分数为 ×100%=52.17%,乙醇的质量为7.2g÷52.17%=13.8g,乙醇中氢元素的质量为13.8g×
×100%=52.17%,乙醇的质量为7.2g÷52.17%=13.8g,乙醇中氢元素的质量为13.8g×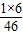 ×100%=1.8g,则生成水中的氢元素也是1.8g,所以水的质量为1.8g÷
×100%=1.8g,则生成水中的氢元素也是1.8g,所以水的质量为1.8g÷ =16.2g.
=16.2g.(4)甲烷和乙醇在燃烧时,它们中的碳都形成二氧化碳了,二者含碳量越高,产生二氧化碳的质量也越大,甲烷中碳碳的质量占
 ,乙醇中碳的质量占
,乙醇中碳的质量占 ,所以产生CO2的质量较多的是甲烷.
,所以产生CO2的质量较多的是甲烷.故答案为:(1)A中的无水硫酸铜由白色变为蓝色;E的玻璃管中黑色的氧化铜变为红色,F中的澄清石灰水变浑浊;
(2)验证产物中CO2的存在;除去CO2;检验CO2是否已除尽;
(3)13.8;16.2;
(4)甲烷.
点评:能源、信息、材料、环境是当今世界四大首要问题,在能源危机日趋严重的今天,新能源的开发和利用,它既是社会热点,也是化学考查的热点,特别是氢能、乙醇汽油等.

练习册系列答案
相关题目
