题目内容
正确的实验操作对人身安全以及实验结果都非常重要.下列实验操作正确的是( )
A、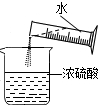 稀释浓硫酸 |
B、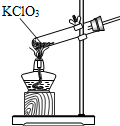 加热氯酸钾固体 |
C、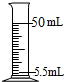 量5.5mL液体 |
D、 检查装置气密性 |
考点:浓硫酸的性质及浓硫酸的稀释,测量容器-量筒,检查装置的气密性,氧气的制取装置
专题:常见仪器及化学实验基本操作
分析:A、根据浓硫酸的稀释方法考虑;
B、根据给试管内固体加热的注意事项考虑;
C、根据量筒的选取方法考虑;
D、根据装置气密性检查方法考虑.
B、根据给试管内固体加热的注意事项考虑;
C、根据量筒的选取方法考虑;
D、根据装置气密性检查方法考虑.
解答:解:
A、稀释浓硫酸时,将浓硫酸沿着烧杯壁慢慢的倒入水中,并用玻璃棒搅拌,故A错;
B、试管内固题加热,试管口要低于试管底,防止冷凝水倒流入试管将试管炸裂,故B错;
C、选取量筒时,要选择比量取到的液体量大,且最接近的,所以应该选择10mL量筒量取9.5mL液体,故C错;
D、检查装置气密性:连接装置,将导管口浸入水中,用手掌紧握试管外壁,如果有气泡产生,说明气密性良好,故D对.
答案:D.
A、稀释浓硫酸时,将浓硫酸沿着烧杯壁慢慢的倒入水中,并用玻璃棒搅拌,故A错;
B、试管内固题加热,试管口要低于试管底,防止冷凝水倒流入试管将试管炸裂,故B错;
C、选取量筒时,要选择比量取到的液体量大,且最接近的,所以应该选择10mL量筒量取9.5mL液体,故C错;
D、检查装置气密性:连接装置,将导管口浸入水中,用手掌紧握试管外壁,如果有气泡产生,说明气密性良好,故D对.
答案:D.
点评:化学实验的基本操作是做好化学实验的基础,学生要在平时的练习中多操作,掌握操作要领,使操作规范.

练习册系列答案
相关题目
下列叙述中正确的是( )
| A、镁带在空气中燃烧后,生成物的质量跟原镁带的质量相等 |
| B、无数实验证明化学反应都遵循质量守恒定律 |
| C、水受热蒸发,水蒸气的质量等于原液态水的质量,符合质量守恒定律 |
| D、煤球燃烧后质量减轻,这不符合质量守恒定律 |
下列有关资源的叙述正确的是( )
| A、大气资源中性质最稳定的物质是氧气 |
| B、海洋资源中含量最多的金属元素是镁 |
| C、地壳中含量最多的元素是铝 |
| D、人体中含量最多的金属元素是钙 |
除去下列物质中的少量杂质所选用的试剂或方法正确的是( )
| 选项 | 物质 | 所含杂质 | 所选用试剂或方法 |
| A | NaOH溶液 | Na2CO3 溶液 | 稀盐酸 |
| B | CaO | CaCO3 | 高温灼烧 |
| C | Fe | Zn | 稀硫酸 |
| D | 稀盐酸 | 稀硫酸 | 加适量Ba(NO3)2溶液,再过滤 |
| A、A | B、B | C、C | D、D |
Sb2O5是一种重要的阻燃剂,其中Sb元素的化合价是( )
| A、+5 | B、+2 | C、-2 | D、-5 |
下列说法正确的是( )
| A、金刚石和石墨物理性质差异很大的原因是构成物质的原子结构不同 |
| B、人们常常在铁的表面刷一层铝粉防锈,原因是铝的化学性质不活泼 |
| C、盐酸可用于除铁锈,原因是盐酸可与金属氧化物反应 |
| D、把Ca(OH)2和NH4Cl一起使用既可改良土壤酸性又可以补充氮肥 |
关于相对原子质量,下列说法正确的是( )
| A、相对原子质量就是原子质量 |
| B、相对原子质量没有单位 |
| C、通常情况下,相对原子质量是以“千克”为单位 |
| D、相对原子质量≈质子数+中子数 |
下列变化不能通过一步反应实现的是( )
| A、Cu→Cu(OH)2 |
| B、Fe→Cu |
| C、CaCO3→CaCl2 |
| D、Na2CO3→NaOH |