题目内容
(2013?铁岭)实验室中有一包含有少量氧化铜的铜粉.同学们欲测定这包铜粉中单质铜的质量分数.现称取20g样品放入烧杯中,逐滴滴入质量分数为10%的稀硫酸至固体不再减少,共用稀硫酸49g.试计算:这包含有少量氧化铜的铜粉中单质铜的质量分数.
分析:依据铜不能与硫酸反应,而氧化铜能够与硫酸反应生成硫酸铜和水,而后利用所用硫酸的质量利用化学方程式即可求出氧化铜的质量,从而可得氧化铜的质量,据此分析解答即可;
解答:解:稀硫酸中溶质的质量为49g×l0%=4.9g
设氧化铜的质量为x.
H2SO4+CuO═CuSO4+H2O
98 80
4.9g x
=
x=4g
所以混合物中铜单质的质量分数为:
×100%=80%
答:这包含有少量氧化铜的铜粉中单质铜的质量分数是80%.
设氧化铜的质量为x.
H2SO4+CuO═CuSO4+H2O
98 80
4.9g x
| 98 |
| 4.9g |
| 80 |
| x |
x=4g
所以混合物中铜单质的质量分数为:
| 20g-4g |
| 20g |
答:这包含有少量氧化铜的铜粉中单质铜的质量分数是80%.
点评:此题是对化学方程式计算的考查,解题的关键是能够分析出过程中的有关反应和根据化学方程式的基本计算;

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
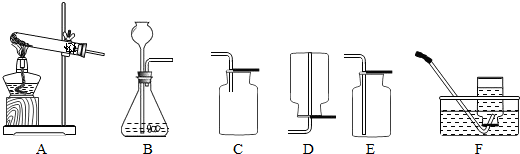
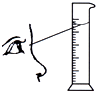 (2013?铁岭)以下是在实验室中用浓硫酸配制稀硫酸时,遇到的几个问题.请回答:
(2013?铁岭)以下是在实验室中用浓硫酸配制稀硫酸时,遇到的几个问题.请回答: