题目内容
【题目】某同学设计如下实验,测定某品牌碳酸饮料中CO2的含量,设计如下实验步骤: 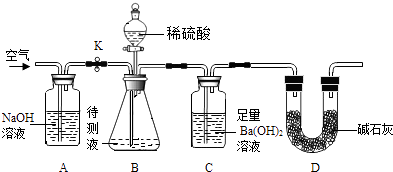
①将250mL瓶装碳酸饮料放在冰箱中冷冻一段时间(未结冰);
②将饮料从冰箱内取出,迅速加入质量分数为50%NaOH溶液5mL;倒转饮料瓶,轻轻震荡,然后放置恢复至室温,作待测液;
③按如图连接实验装置.取50mL待测液置于装置B的锥形瓶中,关闭开关K,打开分液漏斗的活塞,向锥形瓶中注入稀硫酸,至不再产生气泡,关闭活塞;
④打开开关K,向装置中鼓入空气,一段时间后,将C装置中的物质过滤,洗涤,烘干称量质量为0.394g.
资料:
①CO2与足量Ba(OH)2反应生成BaCO3沉淀.
②碱石灰是CaO与NaOH的固体混合物.
③实验中各种溶液的密度都视为1g/mL.
根据以上实验过程完成下列问题:
(1)上述实验过程中,C装置中的现象是 .
(2)装置A中发生的化学反应方程式为 , 装置D的目的是 .
(3)步骤①冷冻碳酸饮料的目的是 .
(4)步骤④鼓入空气的目的是 .
(5)根据题中提供的数据计算此品牌碳酸饮料中CO2的含量为g/L.(加入的NaOH溶液的体积可忽略不计)
【答案】
(1)产生气泡,溶液变浑浊
(2)2NaOH+CO2═Na2CO3+H2O;防止空气中的二氧化碳进入氢氧化钡溶液中
(3)防止二氧化碳逸出
(4)使反应生成的二氧化碳全部被氢氧化钡溶液吸收
(5)1.76
【解析】解:(1)上述实验过程中,除去二氧化碳的空气不溶于氢氧化钡溶液,产生气泡,反应生成的二氧化碳能和氢氧化钡反应生成碳酸钡沉淀,因此C装置中的现象是产生气泡,溶液变浑浊.故填:产生气泡,溶液变浑浊.(2)装置A中,氢氧化钠能和二氧化碳反应生成碳酸钠和水,发生的化学反应方程式为:2NaOH+CO2═Na2CO3+H2O;装置D的目的是防止空气中的二氧化碳进入氢氧化钡溶液中.故填:2NaOH+CO2═Na2CO3+H2O;防止空气中的二氧化碳进入氢氧化钡溶液中.(3)步骤①冷冻碳酸饮料的目的是增大二氧化碳的溶解度,防止二氧化碳逸出.故填:防止二氧化碳逸出.(4)步骤④鼓入空气的目的是使反应生成的二氧化碳全部被氢氧化钡溶液吸收.故填:使反应生成的二氧化碳全部被氢氧化钡溶液吸收.(5)设二氧化碳的质量为x,
Ba(OH)2+ | CO2═ | BaCO3↓+H2O |
44 | 197 | |
x | 0.394g |
![]() =
= ![]() ,
,
x=0.088g,
此品牌碳酸饮料中CO2的含量为:0.088g/50mL=0.088g/0.05L=1.76g/L.
故填:1.76.
【考点精析】本题主要考查了二氧化碳的化学性质和书写化学方程式、文字表达式、电离方程式的相关知识点,需要掌握化学性质:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸;与水反应生成碳酸;能使澄清的石灰水变浑浊;与灼热的碳反应;注意:a、配平 b、条件 c、箭号才能正确解答此题.

【题目】“舌尖上的中国”在央视上的热播让厨房再次成为人们施展厨艺的物态.大多数厨师有个工作经验:炒菜时,又加料酒又加醋,可使菜变得香美可口,原因是醋中的乙酸与料酒之中的乙醇生成乙酸乙酯.如表中是几种常见的酯,请完成下列问题:
酯的名称 | 甲酸甲酯 | 甲酸乙酯 | 乙酸甲酯 | 乙酸乙酯 |
化学式 | C2H4O2 | C3H6O2 | C3H6O2 | X |
(1)甲酸甲酯(C2H4O2)中碳元素、氢元素、氧元素的质量比为;
(2)甲酸乙酯(C3H6O2)中碳元素的质量分数为(计算结果精确到0.1%);
(3)比较归纳是学习化学的重要方法,据表推测X额定化学式为 .