题目内容
把4g硫粉分别放在给定质量的氧气中燃烧,有关实验数据如下表所示.| 第一次 | 第二次 | 第三次 | |
| O2质量(g) | 3 | 4 | 6 |
| SO2质量(g) | 6 |
(1)第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比是 ;
(2)在表中填写第二次实验生成二氧化硫的质量 g.
(3)在表中填写第三次生成的二氧化硫的质量 g.
【答案】分析:(1)根据硫与氧气反应的化学方程式和生成的二氧化硫的质量,就可计算出第一次实验中参加反应的硫的质量,进而计算出第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比;
(2)根据硫与氧气反应的化学方程式和参与反应的氧气的质量,即可计算出第二次实验生成二氧化硫的质量;
(3)根据质量守恒定律和(2)中计算出的第二次实验生成二氧化硫的质量,即可计算出第二次反应中参与反应的S的质量为4g,说明,此时硫已完全反应,故第三次生成的二氧化硫的质量为8g.
解答:解:(1)设第一次实验中参加反应的硫的质量为x,
S+O2 SO2
SO2
32 64
x 6g
∴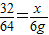
解之得;x=3g;
∴第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比为:3g:3g:6g=1:1:2;
(2)设第二次实验生成二氧化硫的质量为y,
S+O2= SO2
SO2
32 64
4g y
∴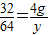
解之得:y=8g;
则参与反应的S的质量为:8g-4g=4g;
(3)因为第二次反应中参与反应的S的质量为4g,说明,此时硫已完全反应,故第三次生成的二氧化硫的质量为8g.
故答案为:(1)1:1:2;(2)8;(3)8.
点评:本题主要考查学生运用化学方程式进行计算的能力.
(2)根据硫与氧气反应的化学方程式和参与反应的氧气的质量,即可计算出第二次实验生成二氧化硫的质量;
(3)根据质量守恒定律和(2)中计算出的第二次实验生成二氧化硫的质量,即可计算出第二次反应中参与反应的S的质量为4g,说明,此时硫已完全反应,故第三次生成的二氧化硫的质量为8g.
解答:解:(1)设第一次实验中参加反应的硫的质量为x,
S+O2
 SO2
SO232 64
x 6g
∴
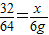
解之得;x=3g;
∴第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比为:3g:3g:6g=1:1:2;
(2)设第二次实验生成二氧化硫的质量为y,
S+O2=
 SO2
SO232 64
4g y
∴
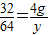
解之得:y=8g;
则参与反应的S的质量为:8g-4g=4g;
(3)因为第二次反应中参与反应的S的质量为4g,说明,此时硫已完全反应,故第三次生成的二氧化硫的质量为8g.
故答案为:(1)1:1:2;(2)8;(3)8.
点评:本题主要考查学生运用化学方程式进行计算的能力.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
把4g硫粉分别放在给定质量的氧气中燃烧,有关实验数据如下表所示.
请回答下列问题:
(1)第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比是 ;
(2)在表中填写第二次实验生成二氧化硫的质量 g.
(3)在表中填写第三次生成的二氧化硫的质量 g.
| 第一次 | 第二次 | 第三次 | |
| O2质量(g) | 3 | 4 | 6 |
| SO2质量(g) | 6 |
(1)第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比是
(2)在表中填写第二次实验生成二氧化硫的质量
(3)在表中填写第三次生成的二氧化硫的质量
把4g硫粉分别放在给定质量的氧气中燃烧,有关实验数据如下表所示.
请回答下列问题:
(1)第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比是 ;
(2)在表中填写第二次实验生成二氧化硫的质量 g.
(3)在表中填写第三次生成的二氧化硫的质量 g.
| 第一次 | 第二次 | 第三次 | |
| O2质量(g) | 3 | 4 | 6 |
| SO2质量(g) | 6 |
(1)第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比是 ;
(2)在表中填写第二次实验生成二氧化硫的质量 g.
(3)在表中填写第三次生成的二氧化硫的质量 g.
把4g硫粉分别放在给定质量的氧气中燃烧,有关实验数据如下表所示.
请回答下列问题:
(1)第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比是 ;
(2)在表中填写第二次实验生成二氧化硫的质量 g.
(3)在表中填写第三次生成的二氧化硫的质量 g.
| 第一次 | 第二次 | 第三次 | |
| O2质量(g) | 3 | 4 | 6 |
| SO2质量(g) | 6 |
(1)第一次实验中参加反应的硫的质量、氧气的质量与生成二氧化硫的质量比是 ;
(2)在表中填写第二次实验生成二氧化硫的质量 g.
(3)在表中填写第三次生成的二氧化硫的质量 g.