题目内容
【题目】现有碳酸钠和氯化钠的固体混合样品。由下图实验过程和提供的数据可计算样品中碳酸钠的质量分数约为

A. 47.5% B. 21.2% C. 70.7% D. 85.6%
【答案】A
【解析】向碳酸钠和氯化钠的固体混合物中,加入盐酸发生的反应为:Na2CO3+2HCl====2NaCl+H20+CO2↑蒸发时,二氧化碳和水逸出,所以所得固体和原固体质量差为碳酸钠和生成氯化钠的质量差,设混合物中碳酸钠的质量为x,则Na2CO3+2HCl====2NaCl+H20+CO2↑ 固体质量差
106 117 11
x 0.55g
106/x=11/0.55g x=5.3g
样品中碳酸钠的质量分数约为5.3g÷11.15g×100%≈47.5% 选A

练习册系列答案
 53天天练系列答案
53天天练系列答案
相关题目
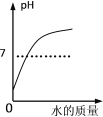
【题目】下列四个图像中,能正确表示对应变化关系的是 (_________)
|
|
|
|
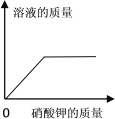
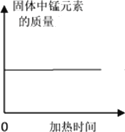
A.向一定量稀盐 酸中加水稀释 | B.一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 | C.加热一定量的 高锰酸钾固体 | D.等质量的铁片、铝片分别与足量且质量分数相同的稀硫酸反应 |
A.A B.B C.C D.D