题目内容
【题目】某校化学兴趣小组用一瓶含有少量氯化钠的硫酸钠固体样品,进行如图所示的实验.

请根据以上信息计算(结果保留到小数点后两位):
(1)反应生成沉淀的质量为 。
(2)样品中氯化钠的质量。
(3)滤液中溶质的质量分数。
【答案】(1)11.65g (2)2.9g (3)6.25%
【解析】
试题分析:硫酸钠和氯化钡反应生成白色沉淀硫酸钡和氯化钠,根据沉淀硫酸钡的质量可以计算硫酸钠的质量和生成的氯化钠的质量,进一步可以计算样品中氯化钠的质量和滤液中溶质的质量分数。
(1)反应生成沉淀的质量为:10.00g+87.00g+54.65g﹣140.00g=11.65g,
(2)设硫酸钠的质量为x,生成氯化钠的质量为y,
BaCl2+Na2SO4═BaSO4↓+2NaCl,
142 233 117
x 11.65g y
![]() ,
,
x=7.1g,y=5.85g,
样品中氯化钠的质量为:10.00g﹣7.1g=2.9g,
(3)滤液中溶质的质量分数为:![]() ×100%=6.25%,
×100%=6.25%,
答:略

【题目】(1)实验室常用氯化铵固体与碱石灰固体共热来制取氨气。常温下NH3是一种无色、有刺激性气味的气体,密度比空气小。NH3极易溶于水,其水溶液呈碱性。

Ⅰ.制取氨气反应的方程式:2NH4Cl+Ca(OH)2=CaCl2+2NH3↑+2X。X的化学式为_____________。
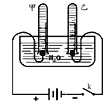
Ⅱ.制取并收集NH3,应该从上图中选择的发生装置是______,收集装置是_______。
Ⅲ.NH3是一种碱性气体,干燥时不能选用下列干燥剂中的______(填序号)。
A.固体氢氧化钠 B.浓硫酸 C.生石灰
(2)刘廷在实验室找到一瓶长期放置的NaOH溶液,欲对其成分进行实验探究。
【收集资料】
Ⅰ.NaOH与CO2分两步反应:2NaOH+CO2=Na2CO3+H2O;
Na2CO3+CO2+H2O= 2NaHCO3
Ⅱ.NaOH与 NaHCO3反应方程式为:NaOH+ NaHCO3=Na2CO3+H2O
Ⅲ.溶液的酸碱性:BaCl2溶液呈中性,其他物质的溶解性见下表
|
|
| |
| 不溶 | 溶 | 溶 |
【提出猜想】刘廷根据资料中的Ⅰ、Ⅱ对其成分提出了以下合理猜想,请将猜想补充完整
猜想1:只有NaOH, 猜想2:只有Na2CO3, 猜想3:只有 NaHCO3
你认为还有可能是______________。
【实验验证】
步骤 | 操作 | 现象 | 结论 |
步骤1 | 取该NaOH溶液,加入过量BaCl | 产生白色沉淀 | p>证明________不成立(填数字) |
步骤2 | 取步骤1中上层清液, 滴加________ | 无气泡产生 | 证明原溶液不含________(填“离子”) |
步骤3 | 另取步骤1中上层清液, 滴加________ | 溶液未变红 | 证明原溶液不含________(填“离子”) |
【实验结论】
通过以上实验操作得出结论:猜想_________是正确的(填数字)。