题目内容
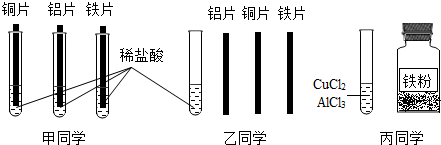
(2012?锦州)如图是五种粒子的结构示意图,请回答下列问题:

(1)在化学反应中,容易失去电子的是
(2)属于同种元素的粒子是
(3)若D带有2个单位的正电荷,则X=

(1)在化学反应中,容易失去电子的是
C
C
(填字母),(2)属于同种元素的粒子是
AE
AE
(填字母);(3)若D带有2个单位的正电荷,则X=
12
12
.分析:(1)根据原子结构中最外层的电子数与元素的性质之间的关系分析;
(2)根据元素的定义分析;
(3)在原子中核内质子数等于核外电子数.
(2)根据元素的定义分析;
(3)在原子中核内质子数等于核外电子数.
解答:解:(1)由五种粒子的结构示意图中可知,在C的结构示意图中,最层的电子数是1,少于4个,在化学反应中,容易失去电子;
(2)有元素的定义可知,五种粒子的结构示意图中,AE的质子数相同都是8,属于同种元素;
(3)由题意可知,若D带有2个单位的正电荷,则D的原子中核外有12个电子,则核内的质子数X是12.
故答为:(1)C; (2)A、E; (3)12.
(2)有元素的定义可知,五种粒子的结构示意图中,AE的质子数相同都是8,属于同种元素;
(3)由题意可知,若D带有2个单位的正电荷,则D的原子中核外有12个电子,则核内的质子数X是12.
故答为:(1)C; (2)A、E; (3)12.
点评:掌握元素的概念:具有相同核电荷数(即质子数)的一类原子总称,以及原子的结构特点是解题的关键.

练习册系列答案
相关题目
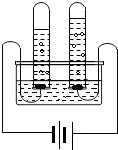 (2012?锦州)生活中处处有化学,请用相关的知识回答下列问题:
(2012?锦州)生活中处处有化学,请用相关的知识回答下列问题: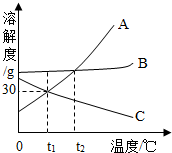 (2012?锦州)如图是A、B、C三种物质的溶解度曲线.看图回答问题:
(2012?锦州)如图是A、B、C三种物质的溶解度曲线.看图回答问题: