题目内容
【题目】向50g氯化氢和氯化钠的混合溶液中滴加溶质质量分数为20%的氢氧化钠溶液,得到溶液的pH变化曲线如图所示,请回答下列问题: 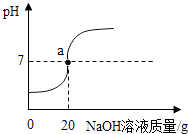
(1)曲线上a点所表示的意义是
(2)计算该50%混合溶液中溶质氯化氢的质量.
(3)若已知50%混合溶液中含氯化钠8.15g,则a点所得溶液的溶质质量分数是多少?
【答案】
(1)盐酸和氢氧化钠恰好完全反应
(2)解:设氯化氢的质量为x
NaOH+HCl=NaCl+H2O
40 36.5
20g×20% x
![]() =
= ![]()
x=3.65g
(3)解:所得溶液的溶质质量分数为: ![]() ×100%=11.6%
×100%=11.6%
【解析】解:(1)a点的pH值等于7,说明盐酸和氢氧化钠恰好完全反应;
【考点精析】通过灵活运用根据化学反应方程式的计算,掌握各物质间质量比=系数×相对分子质量之比即可以解答此题.

练习册系列答案
相关题目