题目内容
【题目】工业上用石灰石浆吸收废气中的二氧化硫,并制取石膏(主要成分为硫酸钙).主要流程如图所示: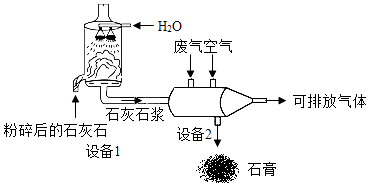
(1)设备1中,石灰石加水制成石灰石浆的目的是 . 设备2中的主要反应为:2CaCO3+2SO2+O2═2CaSO4+2X,则X的化学式为 .
(2)按上述方法处理2000t废气中的二氧化硫,至少需要含5t碳酸钙的石灰石浆.计算废气中二氧化硫的质量为 t.
【答案】
(1)增大反应物的接触面积,使石灰石与二氧化硫充分反应;CO2
(2)3.2
【解析】解:(1)设备1中,石灰石加水制成石灰石浆的目的是增大反应物的接触面积,使石灰石与二氧化硫充分反应;
由2CaCO3+2SO2+O2═2CaSO4+2X可知,反应前后钙原子、硫原子的个数都是2个,反应前碳原子是2个,反应后应该是2个,包含在2X中,反应前氧原子个数是12个,反应后应该是12个,其中4个包含在2X中,则X的化学式为CO2 .
故填:增大反应物的接触面积,使石灰石与二氧化硫充分反应;CO2 . (2)设废气中二氧化硫的质量为x,
2CaCO3+ | 2SO2+O2═2CaSO4+2CO2 , |
200 | 128 |
5t | X |
![]() =
= ![]() ,
,
x=3.2t,
故填:3.2.
反应物接触越充分,反应速率越快;
化学反应遵循质量守恒定律,即反应前后元素种类不变,原子种类和总个数不变;
根据反应的化学方程式和碳酸钙的质量可以计算二氧化硫的质量.

练习册系列答案
相关题目