题目内容
【题目】Cu可以形成化合价为+2和+1的化合物,其中+1价化合物称为亚铜化合物。
(1)氢氧化铜的化学式是_____。
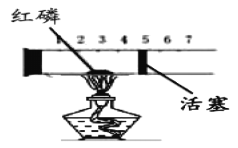
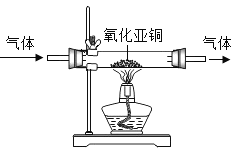
(2)氧化亚铜是一种红色粉末。加热时,氧化亚铜能与氧气发生化合反应,反应的化学方程式_____;利用这一性质可检验氮气中是否含有氧气(装置如图所示),判断氮气中含有氧气的现象是_____。
【答案】Cu(OH)2 2Cu2O+O2![]() 4CuO 固体粉末由红色变为黑色
4CuO 固体粉末由红色变为黑色
【解析】
(1)铜元素通常显+2价,氢氧根显-1,氢氧化铜的化学式是Cu(OH)2。
(2)根据氧化亚铜能与氧气发生化合反应,可知生成氧化亚铜和氧气反应生成氧化铜,反应的化学方程式2Cu2O+O2![]() 4CuO;如果氮气中含有氧气,加热时氧气和红色的氧化亚铜反应生成黑色的氧化铜,观察到的现象是固体粉末由红色变为黑色。
4CuO;如果氮气中含有氧气,加热时氧气和红色的氧化亚铜反应生成黑色的氧化铜,观察到的现象是固体粉末由红色变为黑色。

【题目】氧气是我们身边无法离开的物质。某兴趣小组对氧气进行了一系列研究。
Ⅰ.氧气的制备
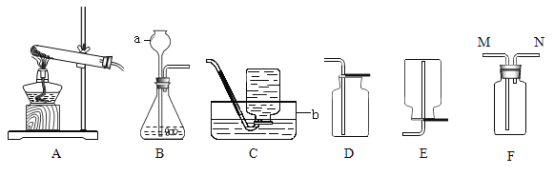
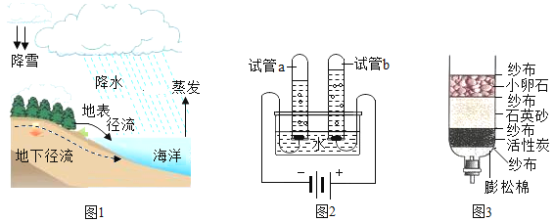
(1)写出图中有标号仪器的名称a__________________,b___________________。
(2)用A装置制取氧气,写出反应的化学方程式:___________________,
(3)用双氧水和二氧化锰制取氧气的化学方程式为_____________________, 反应后过滤、干燥,所得到的二氧化锰____________________(填 “能”或“不能”)继续作为双氧水分解的催化剂。
Ⅱ .氧气的收集
(1)装置C、D、E、F在实验室不能用来收集氧气的是____________________(填字母编号)。
[实验一]用D装置收集氧气,当放置在集气瓶口带火星木条复燃时停止收集,测定瓶中氧气的含量,重复实验三次。
[实验二]用D装置收集氧气,当放置在集气瓶口带火星木条复燃后,继续收集40 秒,测定瓶中氧气的含量,重复实验三次。
[实验三]用排水法收集氧气,测定瓶中氧气的含量,重复实验三次。
实验数据:
实验1 | 实验2 | 实验3 | |||||||
氧气的体积分数(%) | 79.7 | 79.6 | 79.9 | 88.4 | 89.0 | 87.9 | 90.0 | 89.8 | 89.3 |
氧气的平均体积分数(%) | 79.7 | 88.4 | 89.7 | ||||||
数据分析:
(2)由实验1、 2可知,用向上排空气法收集氧气时,为提高获得的氧气体积分数,可采取的措施是___________________,
(3)不考虑操作及药品因素,实验3获得的氧气体积分数不能达到100%的主要原因是____________________。
Ⅲ.铁丝在氧气中燃烧
做完“铁在氧气里燃烧”的实验后,同学们对铁燃烧时溅落下来的黑色物质产生了疑问。
[问题一]铁燃烧时溅落下来的黑色物质中还有没有铁?
[查阅资料1]①氧化亚铁极易被氧化为氧化铁,因此自然界中铁的氧化物主要有氧化铁和四氧化三铁两种:②氧化铁为红棕色固体,不能被磁铁吸引,铁和四氧化三铁能被磁铁吸引;③铁能和稀盐酸反应生成氢气,铁的氧化物也能和稀盐酸反应,但无气体产生。
[实验探究]将铁丝燃烧后得到的黑色物质冷却,然后研碎,________________________,说明溅落下来的黑色物质中含有铁。
[问题二]铁燃烧的产物为什么不是氧化铁呢?
[查阅资料2]
①氧化铁和四氧化三铁分解温度见下表:
②氧化铁高温分解成四氧化三铁。
四氧化三铁 | 氧化铁 | 铁 | |
分解温度/°C | 1538 | 1400 | / |
熔点/°C | / | / | 1535 |
[理论讨论]根据上述探究及实验现象,并结合表中数据分析,可推知铁在氧气里燃烧时产生的高温在___________________________,之间,此温度范围氧化铁已分解。
[拓展延伸]
(1)氧化铁高温分解可生成四氧化三铁和一种气体,写出该反应的化学方程式____________________________,
(2)有些食品包装盒内放有少量黑色的氧化亚铁,若粉末的颜色___________________________,就说明包装盒漏气,售货员就能及时发现并处理。