题目内容
实验内容及相关现象如表所示.
| 实验 编号 |
容器Ⅰ | 分液漏斗Ⅰ | 容器Ⅱ | 分液漏斗Ⅱ | 红墨水液面位置 |
| a | 二氧化碳 (充满) |
10mL澄清 石灰水 |
二氧化碳 (充满) |
10mL水 | 左侧液面升高 右侧液面降低 |
| b | 二氧化碳 (充满) |
10mL澄清 石灰水 |
二氧化碳 (充满) |
10mLA溶液 | 左侧液面降低 右侧液面升高 |
| c | 0.65g锌 | 15mL盐酸 | 0.24g镁 | 15mL盐酸 |
②实验b中,根据红墨水液面位置,推测A溶液可能具有的性质是
③实验c中,盐酸浓度相同且足量,产生气泡更剧烈的是容器
(2)图2所示装置中,容器Ⅲ、Ⅳ体积相同,其中容器Ⅲ中放有植物油,U形管内左右两端红墨水液面相平.实验时分别向Ⅲ、Ⅳ中加入形状和大小相同的铁片,迅速塞紧橡皮塞并放置一段时间.下列说法错误的是
A.植物油用于隔绝氧气和水
B.两支试管中的铁片均被腐蚀
C.U形管右侧液面降低左侧液面升高
D.U形管左侧液面降低右侧液面升高.
金属越活泼,与酸反应时越剧烈;
(2)铁制品与水和氧气同时接触时容易生锈,水和氧气是铁制品生锈的必要条件,缺一不可.
故填:溶液变浑浊;H2O+CO2=H2CO3.
②实验b中,左侧液面降低,右侧液面升高,说明二氧化碳能和A溶液反应,并且反应比二氧化碳和石灰水反应更彻底,或A溶液能够吸收二氧化碳.
故填:能与二氧化碳反应或能够吸收二氧化碳.
③因为镁比锌活泼,所以反应时,镁和稀盐酸反应更剧烈,产生气泡更多;又因为0.65g锌和足量的稀盐酸反应能生成0.02g氢气,0.24g镁和足量的稀盐酸反应能生成0.02g氢气,(通过化学方程式计算可知),所以反应结束并恢复至室温后,红墨水液面位置是两端相平.
故填:Ⅱ;两侧液面相平.
(2)A.植物油用于隔绝氧气和水,该选项说法正确;
B.容器Ⅲ中的铁片没有与水和氧气接触,不能生锈;容器Ⅳ中的铁片与水和氧气接触,能够生锈;该选项说法错误;
C.因为容器Ⅳ中的水蒸气和氧气被消耗,压强减小,容器Ⅲ中的水蒸气和氧气没有被消耗,压强不变,所以U形管左侧液面降低右侧液面升高;该选项说法错误;
D.U形管左侧液面降低右侧液面升高;该选项说法正确.
故填:BC.

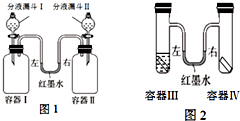
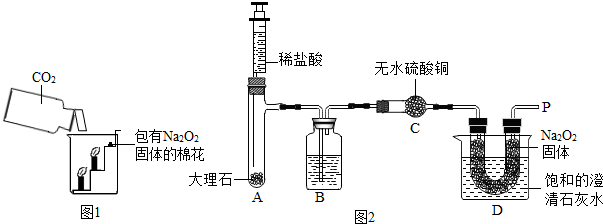
(1)图1所示装置中,容器Ⅰ、II体积相同,U形管内左右两侧液面相平,且装置气密性良好。实验时,打开分液漏斗旋塞,将液体同时滴入容器,滴加完毕后关闭旋塞。实验内容及相关现象如下表所示。

|
实验 编号 |
容器Ⅰ |
分液漏斗Ⅰ |
容器Ⅱ |
分液漏斗Ⅱ |
红墨水液面位置 |
|
a |
二氧化碳 (充满) |
10 mL澄清 石灰水 |
二氧化碳 (充满) |
10 mL水 |
[]左侧液面升高 右侧液面降低 |
|
b |
二氧化碳 (充满) |
10 mL澄清 石灰水 |
二氧化碳 (充满) |
10 mLA溶液 |
左侧液面降低 右侧液面升高 |
|
c |
0.65 g锌 |
15 mL盐酸 |
0.24g镁 |
15 mL盐酸 |
|
实验a中,容器Ⅰ中的现象是________,容器Ⅱ中反应的化学方程式是 。
实验b中,根据红墨水液面位置,推测A溶液可能具有的性质是 。
实验c中,盐酸浓度相同且足量,产生气泡更剧烈的是容器________(填“Ⅰ”或“Ⅱ”);反应结束并恢复至室温后,红墨水液面位置是________。
(2)图2所示装置中,容器III、IV体积相同,其中容器Ⅲ中放有植物油,U形管内左右两端红墨水液面相平。实验时分别向III、IV中加入形状和大小相同的铁片,迅速塞紧橡皮塞并放置一段时间。下列说法错误的是 (填字母序号)。

A.植物油用于隔绝氧气和水
B.两支试管中的铁片均被腐蚀
C.U形管右侧液面降低左侧液面升高
D.U形管左侧液面降低右侧液面升高
(1)图1所示装置中,容器Ⅰ、II体积相同,U形管内左右两侧液面相平,且装置气密性良好。实验时,打开分液漏斗旋塞,将液体同时滴入容器,滴加完毕后关闭旋塞。实验内容及相关现象如下表所示。
| 实验 编号 | 容器Ⅰ | 分液漏斗Ⅰ | 容器Ⅱ | 分液漏斗Ⅱ | 红墨水液面位置 |
| a | 二 (充满) | 10 mL澄清 石灰水 | 二氧化碳 (充满) | 10 mL水 | 左侧液面升高 右侧液面降低 |
| b | 二氧化碳 (充满) | 10 mL澄清 石灰水 | 二氧化碳 (充满) | 10 mLA溶液 | 左侧液面降低 右侧液面升高 |
| c | 0.65 g锌 | 15 mL盐酸 | 0.24 g镁 | 15 mL盐酸 |
① 实验a中,容器Ⅰ中的现象是________,容器Ⅱ中反应的化学方程式是 。
② 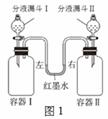 实验b中,根据红墨水液面位置,推测A溶液可能具有
实验b中,根据红墨水液面位置,推测A溶液可能具有
的性质是 。
③ 实验c中,盐酸浓度相同且足量,产生气泡更剧烈的是容
器________(填“Ⅰ”或“Ⅱ”);反应结束并恢复至室温后,红
墨水液面位置是________。
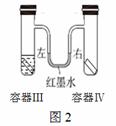 (2)图2所示装置中,容器III、IV体积相同,其中容器Ⅲ中放有植物油,U形管内左右两端红墨水液面相平。实验时分别向III、IV中加入形状和大小相同的铁片,迅速塞紧橡皮塞并放置一段时间。下列说法错误的是 (填字母序号)。
(2)图2所示装置中,容器III、IV体积相同,其中容器Ⅲ中放有植物油,U形管内左右两端红墨水液面相平。实验时分别向III、IV中加入形状和大小相同的铁片,迅速塞紧橡皮塞并放置一段时间。下列说法错误的是 (填字母序号)。
A.植物油用于隔绝氧气和水
B.两支试管中的铁片均被腐蚀
C.U形管右侧液面降低左侧液面升高
D.U形管左侧液面降低右侧液面升高
 氧化碳
氧化碳