题目内容
为了探究铁和硫酸铜溶液反应中量的关系,某兴趣小组做了五组实验,实验结果记录如下:
|
编号 |
加入铁的质量/g |
硫酸铜溶液体积/mL |
生成铜的质量/g |
|
1 |
1.12 |
10.0 |
1.28 |
|
2 |
x |
10.0 |
2.56 |
|
3 |
3.36[ |
10.0 |
3.84 |
|
4 |
4.48 |
10.0 |
4.98 |
|
5 |
5.60 |
20.0 |
y |
则表格中记录的x和y的数值应分别为
A.2.24、4.98 B.2.24、6.40 C.3.36、5.12 D.3.36、4.98
【答案】
B
【解析】由表可知1.12g铁和10g硫酸铜生成1.28g铜,因此x=1.12g+1.12g=2.24g,由第四次反应可知,铁没有全部反应了,第四次反应了的铁的质量=
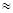 1g,剩余铁的质量=1.12-1=0.12g,第五次反应的铁的质量为0.12+1.12=1.24g,生成铜的质量=
1g,剩余铁的质量=1.12-1=0.12g,第五次反应的铁的质量为0.12+1.12=1.24g,生成铜的质量=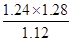
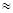 1.42g,y=1.42+4.98=6.40g,故选B
1.42g,y=1.42+4.98=6.40g,故选B

练习册系列答案
相关题目
为了探究铁和铜的金属活动性强弱,请根据实验室现有的仪器和药品条件(如下所列),通过填写下表,完成对实验方案的构思.
实验药品:试管、胶头滴管、镊子
实验仪器:铁钉、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液、硫酸铜溶
实验药品:试管、胶头滴管、镊子
实验仪器:铁钉、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液、硫酸铜溶
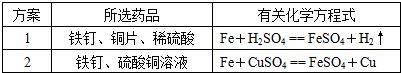
| 方案 | 所选药品 | 有关化学方程式 |
| 1 | 铁钉、铜片、稀硫酸 | Fe+H2SO4 ═FeSO4+H2↑ |
| 2 | 铁钉、硫酸铜溶液 | Fe+CuSO4 ═FeSO4+Cu |
为了探究铁和铜的金属活动性强弱,请根据实验室现有的仪器和药品条件(如下所列),通过填写下表,完成对实验方案的构思.
实验药品:试管、胶头滴管、镊子
实验仪器:铁钉、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液、硫酸铜溶
实验药品:试管、胶头滴管、镊子
实验仪器:铁钉、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液、硫酸铜溶
| 方案 | 所选药品 | 有关化学方程式 |
| 1 | 铁钉、铜片、稀硫酸 | Fe+H2SO4 ═FeSO4+H2↑ |
| 2 | 铁钉、硫酸铜溶液 | Fe+CuSO4 ═FeSO4+Cu |
为了探究铁和硫酸铜溶液反应中量的关系,某兴趣小组做了五组实验,实验结果记录如下:
编号 | 加入铁的质量/g | 硫酸铜溶液体/mL | 生成铜的质量/g |
l | 1.12 | 10.0 | 1.28 |
2 | X | 10.0 | 2.56 |
3 | 3.36 | 10.0 | 3.84 |
4 | 4.48 | 10.0 | 4.98 |
5 | 5.60 | 20.0 | y |
则表格中记录的x和Y的数值应分别为 ( )
A.2.24,4.98 B.2.24,6.40
C.3.36,5.12 D.3.36,4.98