题目内容
 如图标出的是有关热水瓶的组成物质,请回答下列问题.
如图标出的是有关热水瓶的组成物质,请回答下列问题.(1)所标物质中为金属材料的是
铝薄片
铝薄片
(写一种即可),为有机合成材料的是塑料
塑料
.(2)使用一段时间后,瓶胆内壁有水垢出现,这是因为水的硬度较大的缘故.我们可以用
肥皂水
肥皂水
鉴别硬水与软水.生活中通过加热煮沸
加热煮沸
可以降低水的硬度.(3)目前自来水厂,使用一种新型的自来水消毒剂X进行消毒,工业上制取X 的化学方程式为:Cl2+2NaClO2═2NaCl+2X,则X的化学式为
ClO2
ClO2
.(4)可用厨房中的一种常用物质(写名称)
食醋
食醋
除去瓶胆内壁的水垢[已知水垢的主要成分是CaCO3和Mg(OH)2].分析:根据物质的性质进行分析,铝和不锈钢属于金属材料,塑料属于有机合成材料,硬水和软水可以使用肥皂水鉴别,硬水中含有的可溶性钙镁化合物受热易分解生成不溶于水的钙镁化合物,根据质量守恒定律可以推知物质的化学式,食醋具有酸的性质,能用于清除水垢.
解答:解:(1)所标物质中为金属材料的是铝薄片和不锈钢,为有机合成材料的是塑料,故填:铝薄片,塑料;
(2)鉴别硬水和软水可以使用肥皂水,生活中可以使用加热煮沸的方法降低水的硬度,故填:肥皂水,加热煮沸;
(3)根据Cl2+2NaClO2═2NaCl+2X和质量守恒定律的实质,可知X中含有一个氯原子和两个氧原子,是二氧化氯,故填:ClO2;
(4)厨房中的食醋具有酸的性质,能与碳酸钙和氢氧化镁反应生成易溶于水的物质,从而除去水垢,故填:食醋.
(2)鉴别硬水和软水可以使用肥皂水,生活中可以使用加热煮沸的方法降低水的硬度,故填:肥皂水,加热煮沸;
(3)根据Cl2+2NaClO2═2NaCl+2X和质量守恒定律的实质,可知X中含有一个氯原子和两个氧原子,是二氧化氯,故填:ClO2;
(4)厨房中的食醋具有酸的性质,能与碳酸钙和氢氧化镁反应生成易溶于水的物质,从而除去水垢,故填:食醋.
点评:本题考查了常见物质的性质,完成此题,可以依据已有的知识进行.要求同学们加强对基础知识的储备,以便灵活应用.

练习册系列答案
相关题目
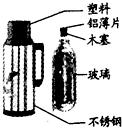 23、如图标出的是有关热水瓶的组成物质,请回答下列问题.
23、如图标出的是有关热水瓶的组成物质,请回答下列问题. 15、如图标出的是有关热水瓶的组成物质,请回答下列问题.
15、如图标出的是有关热水瓶的组成物质,请回答下列问题.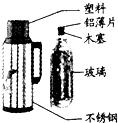 20、如图标出的是有关热水瓶的组成物质,请回答下列问题.
20、如图标出的是有关热水瓶的组成物质,请回答下列问题.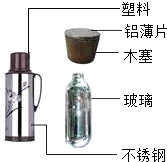 (2011?鄂尔多斯)如图标出的是有关热水瓶的组成物质,请回答下列问题.
(2011?鄂尔多斯)如图标出的是有关热水瓶的组成物质,请回答下列问题.