题目内容
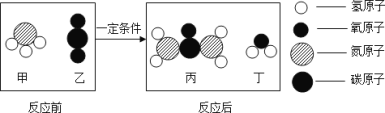
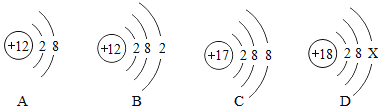
【题目】A、B、C、D为初中化学常见的四种物质,A、B、C、D中均含有一种相同的元素,常温下,A为无色液体,C为黑色固体,它们之间有如图所示的转化和反应关系(“→”表示某一种物质经一步反应可转化为另一种物质,“—”表示相连两物质能发生化学反应,部分反应物、生成物及反应条件已略去)

(1)A的化学式为__________,
(2)C与D发生的化学反应___________。
【答案】H2O CO+CuO![]() Cu+CO2或 4CO+Fe3O4
Cu+CO2或 4CO+Fe3O4![]() 3Fe+4CO2
3Fe+4CO2
【解析】
A、B、C、D为初中化学常见的四种物质,A、B、C、D中均含有一种相同的元素,常温下,A为无色液体,A和B会相互转化,氢气在氧气燃烧生成水,水通电分解生成氢气和氧气,A可能是水,B可能是氧气,C为黑色固体,B会生成C,铁(或铜)与氧气反应生成黑色的四氧化三铁(或氧化铜),C可能是四氧化三铁(或氧化铜),C 与D能反应,根据A、B、C、D中均含有一种相同的元素,D中含有氧元素,四氧化三铁(或氧化铜)能与一氧化碳反应生成铁(或铜)和二氧化碳,D是一氧化碳,经过验证,推导正确。
根据以上分析可知:
(1)A是水,化学式为:H2O;
(2)C与D发生的化学反应可以是四氧化三铁(或氧化铜)和一氧化碳在加热的条件下生成铜(或铁)和二氧化碳,化学方程式分别为:4CO+Fe3O4![]() 3Fe+4CO2或CO+CuO
3Fe+4CO2或CO+CuO![]() Cu+CO2。
Cu+CO2。

【题目】常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见的氧化物和一种气体。小梅很好奇,设计如下实验探究铁粉与水蒸气反应后的产物。

⑴试管尾部放一团棉花的目的是_______________
⑵探究生成的气体是什么?用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中。
⑶探究试管中剩余固体成分是什么?
(查阅资料)
常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
能否被磁铁吸引 | 否 | 否 | 能 |
FeO+2HCl=FeCl2+H2O Fe2O3+6HCl=2FeCl3+3H2O Fe3O4+8HCl=2FeCl2+FeCl3+4H2O
(初步验证)试管中剩余固体为黑色,能全部被磁铁吸引。
(猜想与假设)猜想一:剩余固体是Fe与Fe3O4 ;猜想二:剩余固体是_________________。
(实验探究)
实验操作 | 实验现象及结论 |
向试管中加入_________ | 若_________。则猜想二正确,猜想一不正确。 |
(实验结论)根据⑵和⑶,铁和水蒸气在高温下反应的产物为______________。