��Ŀ����
��2013?������һģ���������������Ʒ��ij��ȤС��ͬѧ��ijƷ����������չ������̽������ش����⣺
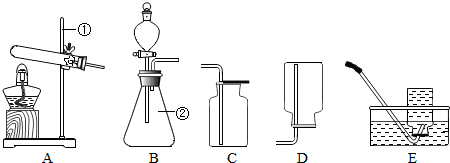
[���Ͽ�Ƭ]��
a��SiO2������ˮ���Ҳ����ᷴӦ�����²��ֽ⣻
b��NaHCO3�����ֽ⣬����Na2CO3��H2O��CO2��
c�������б�ʪ�������������㾫�Ⱦ�Ϊ�л��
��1��ȡһС�����࣬��������ˮ����ֽ�����ã�������ϲ���Һ��pHΪ8.3�����������
��2��С��ͬѧ���֣���Ʒ�������ڶ�������ֿ�����������������ʾ�������е�K12��һ�����Σ���������K12���ܽ�Ⱥ��¶ȵĹ�ϵ��
��3��Ϊ�ⶨ��������SiO2��������������ȤС��ͬѧ��������·�������������3��ʵ�飺
[ʵ�鲽��]��
��ȷ��ȡ2.0g������壬���ˮ�֣����¼��ȣ����������ټ���Ϊֹ���ڸ���������ȴ�����£�
��ת��ʣ�������ձ��У�����ϡHCl����
�۹��ˡ�ϴ�ӡ������õ�ʣ������������������
�ܸ���ʵ�����ݽ��м��㣮
[���ݴ���]��
��4���˲ⶨ��3��ʵ���Ŀ����
��5���ۺ�����ʵ�鷽����ʵ�����ݣ������������SiO2������������
[ʵ�����]��
��6��������ʵ�鲽����������ֲⶨ���ƫ����ƫ���ԭ�������
��7�����¼��ȵ�Ŀ�ij�Ϊ�˳�ȥCaCO3��NaHCO3���⣬��Ϊ��ȥ
��8��������У���ϡHCl�����ķ�Ӧ��
��9��������У�ϴ�ӵ�Ŀ����
��10��Ϊ��֤ϴ��Ч���������
A������ˮ B������ˮ C������NaCl��Һ D������CaCl2��Һ��
 |
���ϱ� |
| Ħ������SiO2��20%�� CaCO3�������� ������NaHCO3��15%�� ���ݼ���K12���������� ��ʪ�������͵ȣ�60%�� ���������������� �������㾫��ˮ�� |
a��SiO2������ˮ���Ҳ����ᷴӦ�����²��ֽ⣻
b��NaHCO3�����ֽ⣬����Na2CO3��H2O��CO2��
c�������б�ʪ�������������㾫�Ⱦ�Ϊ�л��
��1��ȡһС�����࣬��������ˮ����ֽ�����ã�������ϲ���Һ��pHΪ8.3�����������
��
��
�ԣ�ʵ�����ܷ���pH��ֽ��ø���ֵ�����������жϲ�˵�����ɣ����ܣ���ΪpH��ֻֽ�ܲⶨ������ֵ
���ܣ���ΪpH��ֻֽ�ܲⶨ������ֵ
����2��С��ͬѧ���֣���Ʒ�������ڶ�������ֿ�����������������ʾ�������е�K12��һ�����Σ���������K12���ܽ�Ⱥ��¶ȵĹ�ϵ��
K12���ܽ�����¶Ƚ��Ͷ����ͣ������¶����߶�����
K12���ܽ�����¶Ƚ��Ͷ����ͣ������¶����߶�����
����3��Ϊ�ⶨ��������SiO2��������������ȤС��ͬѧ��������·�������������3��ʵ�飺
[ʵ�鲽��]��
��ȷ��ȡ2.0g������壬���ˮ�֣����¼��ȣ����������ټ���Ϊֹ���ڸ���������ȴ�����£�
��ת��ʣ�������ձ��У�����ϡHCl����
���岻�ٲ���Ϊֹ
���岻�ٲ���Ϊֹ
���۹��ˡ�ϴ�ӡ������õ�ʣ������������������
| ʵ���� | 1 | 2 | 3 |
| ʵ��ǰ��g�� | 2.00 | 2.00 | 2.00 |
| ʵ���g�� | 0.43 | 0.44 | 0.45 |
[���ݴ���]��
��4���˲ⶨ��3��ʵ���Ŀ����
���ʵ��ľ�ȷ�ȣ�����Ŷȣ�
���ʵ��ľ�ȷ�ȣ�����Ŷȣ�
����5���ۺ�����ʵ�鷽����ʵ�����ݣ������������SiO2������������
22%
22%
��[ʵ�����]��
��6��������ʵ�鲽����������ֲⶨ���ƫ����ƫ���ԭ�������
������У�û�н�ʣ�������и����ϴ��Һ�����ڹ������
������У�û�н�ʣ�������и����ϴ��Һ�����ڹ������
����7�����¼��ȵ�Ŀ�ij�Ϊ�˳�ȥCaCO3��NaHCO3���⣬��Ϊ��ȥ
��ʪ�������������㾫���л���
��ʪ�������������㾫���л���
����8��������У���ϡHCl�����ķ�Ӧ��
CaO+2HCl�TCaCl2+H2O
CaO+2HCl�TCaCl2+H2O
��Na2CO3+2HCl�T2NaCl+H2O+CO2��
Na2CO3+2HCl�T2NaCl+H2O+CO2��
����9��������У�ϴ�ӵ�Ŀ����
��ȥ������渽�ŵ�CaCl2��NaCl��Һ
��ȥ������渽�ŵ�CaCl2��NaCl��Һ
������ϴ�ӣ���ⶨ�����ƫ��
ƫ��
�����ƫ����ƫС�����䡱����10��Ϊ��֤ϴ��Ч���������
A
A
ϴ�ӣ�A������ˮ B������ˮ C������NaCl��Һ D������CaCl2��Һ��
��������1�����ݲ�����ϲ���Һ��pHΪ8.3����7���н��
��2�����������е�K12�ڶ����������н��
��3������̼���ƺ����ᷴӦ���ɶ�����̼���н��
��4�����ݴ˲ⶨ��3��ʵ���Ŀ�������ʵ��ľ�ȷ�Ƚ��н��
��5������ʣ�������������Ƕ���������������н��
��6�����ݲ�����У�û�н�ʣ�������и����ϴ��Һ�����ڹ��������н��
��7�����ݱ�ʪ�������������㾫���л�����Ȼ�ӷ����н��
��8�����ݢ��еĹ����ж������衢�����ơ�̼���ƽ��н��н��
��9������ϴ�ӵ�Ŀ���dz�ȥ������渽�ŵ�CaCl2��NaCl��Һ���н��
��10����������ˮ�в������������������ʽ��н��
��2�����������е�K12�ڶ����������н��
��3������̼���ƺ����ᷴӦ���ɶ�����̼���н��
��4�����ݴ˲ⶨ��3��ʵ���Ŀ�������ʵ��ľ�ȷ�Ƚ��н��
��5������ʣ�������������Ƕ���������������н��
��6�����ݲ�����У�û�н�ʣ�������и����ϴ��Һ�����ڹ��������н��
��7�����ݱ�ʪ�������������㾫���л�����Ȼ�ӷ����н��
��8�����ݢ��еĹ����ж������衢�����ơ�̼���ƽ��н��н��
��9������ϴ�ӵ�Ŀ���dz�ȥ������渽�ŵ�CaCl2��NaCl��Һ���н��
��10����������ˮ�в������������������ʽ��н��
����⣺��1��������ϲ���Һ��pHΪ8.3����7��������������������ԣ�pH��ֻֽ�ܲⶨ������ֵ���������Һ��pHΪ8.3������ʵ���Ҳ�����pH��ֽ��ø���ֵ��
��2�������е�K12�ڶ���������˵��K12���ܽ�����¶Ƚ��Ͷ����ͣ������¶����߶�����
��3��̼���ƺ����ᷴӦ���ɶ�����̼������ת��ʣ�������ձ��У�����ϡHCl�������岻�ٲ���Ϊֹ��
��4���˲ⶨ��3��ʵ���Ŀ�������ʵ��ľ�ȷ�ȣ�����Ŷȣ���
��5��ʣ�������������Ƕ��������������3��ʵ������SiO2��ƽ��ֵΪ0.44g��
��������SiO2����������=
��100%=22%��
��6��������У�û�н�ʣ�������и����ϴ��Һ�����ڹ�����棬��ʹ�òⶨ���ƫ��
��7����ʪ�������������㾫���л�����Ȼ�ӷ������Ը��¼��ȵ�Ŀ�ij�Ϊ�˳�ȥCaCO3��NaHCO3���⣬��Ϊ��ȥ��ʪ�������������㾫���л��
��8�����еĹ����ж������衢�����ơ�̼���ƣ����Լ�ϡHCl�����ķ�Ӧ�������ƺ����ᷴӦ�����Ȼ��ƺ�ˮ���Լ�̼���ƺ����ᷴӦ�����Ȼ��ơ�ˮ��������̼����ѧ����ʽ�ֱ�ΪCaO+2HCl�TCaCl2+H2O��Na2CO3+2HCl�T2NaCl+H2O+CO2����
��9��ϴ�ӵ�Ŀ���dz�ȥ������渽�ŵ�CaCl2��NaCl��Һ������ϴ�ӣ���ⶨ�����ƫ��
��10������ˮ�в������������������ʣ�����Ϊ��֤ϴ��Ч�������������ˮϴ�ӣ�
�ʴ�Ϊ����1�������ԣ����ܣ���ΪpH��ֻֽ�ܲⶨ������ֵ��
��2��K12���ܽ�����¶Ƚ��Ͷ����ͣ������¶����߶�����
��3�����岻�ٲ���Ϊֹ��
��4�����ʵ��ľ�ȷ�ȣ�����Ŷȣ���
��5��22%��
��6��������У�û�н�ʣ�������и����ϴ��Һ�����ڹ�����棻
��7����ʪ�������������㾫���л��
��8��CaO+2HCl�TCaCl2+H2O��Na2CO3+2HCl�T2NaCl+H2O+CO2����
��9����ȥ������渽�ŵ�CaCl2��NaCl��Һ��ƫ��
��10��A��
��2�������е�K12�ڶ���������˵��K12���ܽ�����¶Ƚ��Ͷ����ͣ������¶����߶�����
��3��̼���ƺ����ᷴӦ���ɶ�����̼������ת��ʣ�������ձ��У�����ϡHCl�������岻�ٲ���Ϊֹ��
��4���˲ⶨ��3��ʵ���Ŀ�������ʵ��ľ�ȷ�ȣ�����Ŷȣ���
��5��ʣ�������������Ƕ��������������3��ʵ������SiO2��ƽ��ֵΪ0.44g��
��������SiO2����������=
| 0.44g |
| 2.0g |
��6��������У�û�н�ʣ�������и����ϴ��Һ�����ڹ�����棬��ʹ�òⶨ���ƫ��
��7����ʪ�������������㾫���л�����Ȼ�ӷ������Ը��¼��ȵ�Ŀ�ij�Ϊ�˳�ȥCaCO3��NaHCO3���⣬��Ϊ��ȥ��ʪ�������������㾫���л��
��8�����еĹ����ж������衢�����ơ�̼���ƣ����Լ�ϡHCl�����ķ�Ӧ�������ƺ����ᷴӦ�����Ȼ��ƺ�ˮ���Լ�̼���ƺ����ᷴӦ�����Ȼ��ơ�ˮ��������̼����ѧ����ʽ�ֱ�ΪCaO+2HCl�TCaCl2+H2O��Na2CO3+2HCl�T2NaCl+H2O+CO2����
��9��ϴ�ӵ�Ŀ���dz�ȥ������渽�ŵ�CaCl2��NaCl��Һ������ϴ�ӣ���ⶨ�����ƫ��
��10������ˮ�в������������������ʣ�����Ϊ��֤ϴ��Ч�������������ˮϴ�ӣ�
�ʴ�Ϊ����1�������ԣ����ܣ���ΪpH��ֻֽ�ܲⶨ������ֵ��
��2��K12���ܽ�����¶Ƚ��Ͷ����ͣ������¶����߶�����
��3�����岻�ٲ���Ϊֹ��
��4�����ʵ��ľ�ȷ�ȣ�����Ŷȣ���
��5��22%��
��6��������У�û�н�ʣ�������и����ϴ��Һ�����ڹ�����棻
��7����ʪ�������������㾫���л��
��8��CaO+2HCl�TCaCl2+H2O��Na2CO3+2HCl�T2NaCl+H2O+CO2����
��9����ȥ������渽�ŵ�CaCl2��NaCl��Һ��ƫ��
��10��A��
����������������������ѧ�Ļ�ѧ֪ʶ�����ʵ���ɡ�̼��ƺ�ϡ����ķ�Ӧ��������̼���������Ƶķ�Ӧ���飬Ҫ����������Щ֪ʶ����д��ѧ����ʽһ��Ҫȷ����

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
 ��2013?������һģ����ͼΪ���������ʵ��ܽ�����ߣ�����˵������ȷ���ǣ�������
��2013?������һģ����ͼΪ���������ʵ��ܽ�����ߣ�����˵������ȷ���ǣ�������